题目内容
7.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转.请回答: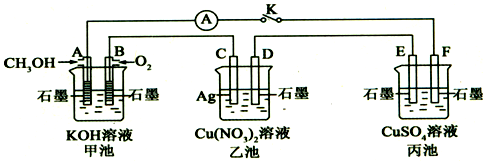
(1)甲池为原电池(填“原电池”、“电解池”或“电镀池”),甲池的PH值变小(填变大,变小或不变),A电极的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O.
(2)丙池中F电极为阴极 (填“正极”、“负极”、“阴极”或“阳极”),
丙池中总反应的离子方程式为2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$4H++2Cu+O2↑F电极上的现象为表面析出红色的固体物质
(3)当乙池中C极质量减轻108g时,甲池中B电极理论上消耗O2的体积为5.6L(标况)
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是BD(填选项字母).
A.Cu B.CuO C.Cu(OH)2 D.CuCO3.
分析 甲池为燃料电池,A为负极,B为正极,则乙中C为阳极,D为阴极,阳极上Ag失电子生成银离子,阴极上铜离子得电子生成Cu,结合溶液中离子变化分析,由此解答.
解答 解:(1)由图可知甲图为原电池是一甲醇燃料电池,通甲醇的A为负极、B为正极,电解质溶液为KOH溶液,则A电极反应方程式为:2CH3OH+16OH--12e-═CO32-+12H2O,B电极反应式为:3O2+12e-+6H2O=12OH-,由A、B电极反应式可知氢氧根离子的浓度减小,所以甲池的PH值变小,
故答案为:原电池; 变小;CH3OH+8OH--6e-═CO32-+6H2O;
(2)丙池中E为阳极,电极反应为:4OH--4e-=O2↑+2H2O,F电极为阴极,电极反应为:Cu2++2e-=Cu,故总反应方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑,离子方程式为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$4H++2Cu+O2↑,
故答案为:阴极;2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$4H++2Cu+O2↑;表面析出红色的固体物质;
(3)乙池为电解池,C为阳极电极反应为:Ag-e-=Ag+,D做阴极,电极反应为Cu2++2e-=Cu,乙池中C极质量减轻10.8g,则其物质的量n(Ag)=$\frac{108g}{108g/mol}$=1mol,则转移电子为1mol,故甲池消耗O2为1 mol×$\frac{1}{4}$=0.25mol,所以体积为0.25 mol×22.4L/mol=5.6L,
故答案为:5.6;
(4)一段时间后,断开电键K,要使丙池恢复到反应前浓度,根据2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑可知,需加入CuO或碳酸铜,均与硫酸生成硫酸铜和水,
故答案为:BD.
点评 本题考查了原电池和电解池的相关知识,侧重于电极反应式书写和电子守恒在计算中应用的考查,题目难度中等,考查了学生对原电池和电解池原理的掌握情况.

| 物 质 | 除杂试剂 | 方法 | |
| A | CO( CO2) | NaOH溶液 | 洗气 |
| B | FeCl2溶液( FeCl3) | 足量铜粉 | 过滤 |
| C | KNO3(KCl) | -- | 蒸发结晶 |
| D | Al2O3(Fe2O3) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,液体也不能蒸干 | |
| B. | 可用稀硝酸鉴别MgI2、AgNO3、Na2CO3、NaAlO2四种溶液 | |
| C. | 将Mg(OH)2沉淀转入烧杯中,加足量稀硫酸溶解,加热浓缩、冷却结晶、过滤后得到晶体 | |
| D. | 除去乙酸乙酯中的乙酸杂质:加入氢氧化钠溶液,分液 |
 如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 溶液中电子流向Y→X | |
| B. | 若两电极分别为铁和碳棒,则X为碳棒,Y为铁 | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 若两电极都是金属,则它们的活动性顺序为X>Y |
| A. | 屠呦呦发现抗疟新药青蒿素而获得诺贝尔奖 | |
| B. | 氯气用作自来水的杀菌消毒剂 | |
| C. | 医用消毒酒精中乙醇的浓度(体积分数)为95% | |
| D. | 燃料不完全燃烧排放的CO是大气污染物之一 |
| A. | 0.01 mol/L | B. | 0.015 mol/L | C. | 0.017 mol/L | D. | 0.05 mol/L |
| A. | 高纯度的单晶硅用于制造光导纤维和登月车的光电池 | |
| B. | 石油裂解的主要目的是为了获得短链不饱和烃 | |
| C. | 按照分散质和分散剂所处的状态,可分为9种分散系 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂或生物柴油 |
 ;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.