题目内容
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1 mol H2O所含有的原子数为NA |
| B、常温常压下,32g O2含有的氧原子数为2NA |
| C、常温常压下,11.2L氯气所含的分子数为NA |
| D、1L 0.1mol/L NaCl溶液中所含的Na+为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、水分子是有氢原子和氧原子构成;
B、质量换算物质的量结合氧气分子式计算氧原子数;
C、依据气体摩尔体积的条件应用分析判断;
D、氯化钠是盐完全电离生成钠离子和氯离子.
B、质量换算物质的量结合氧气分子式计算氧原子数;
C、依据气体摩尔体积的条件应用分析判断;
D、氯化钠是盐完全电离生成钠离子和氯离子.
解答:
解:A、1 mol H2O所含有的原子数为3NA,故A错误;
B、32g O2物质的量为1mol,含有的氧原子数为2NA,故B正确;
C、常温常压下,11.2L氯气物质的量不是0.5mol,故C错误;
D、1L 0.1mol/L NaCl溶液中所含的Na+为0.1NA,故D错误;
故选B.
B、32g O2物质的量为1mol,含有的氧原子数为2NA,故B正确;
C、常温常压下,11.2L氯气物质的量不是0.5mol,故C错误;
D、1L 0.1mol/L NaCl溶液中所含的Na+为0.1NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,气体摩尔体积的条件应用,溶液中离子物质的量的计算,题目较简单.

练习册系列答案
相关题目
在常温下10mL pH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是( )
| A、c(A-)=c(K+) |
| B、c(H+)=c(OH-)<c(K+)<c(A-) |
| C、V总≥20mL |
| D、V总≤20mL |
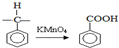
举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )


| A、该分子中所有碳原子可以稳定的共存在一个平面中 |
| B、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| C、1mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4mol、7mol |
| D、滴入酸性KMnO4溶液,观察到紫色褪去,可证明分子中存在双键 |
下列物质的水溶液呈现酸性的是( )
| A、小苏打 | B、生石灰 |
| C、食醋 | D、烧碱 |
下列化学用语表达错误的是( )
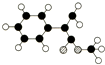
A、乙醇分子的比例模型图: |
| B、苯分子的最简式:CH |
| C、丙烯的结构简式:CH3CHCH2 |
D、甲基的电子式: |
分子和原子的本质区别是( )
| A、分子大原子小 |
| B、分子能保持化学性质原子不能 |
| C、在化学变化中分子可分原子不可分 |
| D、分子能构成物质原子不能 |
用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A、78g过氧化钠晶体中,含2NA个阴离子 |
| B、常温常压下,22.4L氦气含有NA个氦原子 |
| C、在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA |
| D、常温下16g O2与O3的混合气体中含氧原子数为NA |
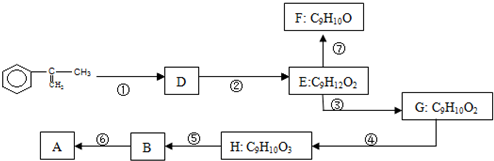
 化学-选修有机化学基础
化学-选修有机化学基础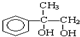 拟从
拟从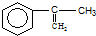 出发合成A.
出发合成A.