题目内容
19.实验室预配置6mol/LH2SO4溶液,不同浓度的硫酸:①240mL1.00mol•L-1的硫酸
②150mL3.00mol•L-1的硫酸
③足量的18.00mol•L-1的浓H2SO4
现有三种规格容量瓶:250mL、500mL、1000mL,配制要求:①、②两种硫酸全部用完不足部分由③补充.请回答下列问题:
(1)选用容量瓶的规格是1000mL.
(2)需要18.00mol•L-1的浓H2SO4的体积是295mL.
分析 ①、②两溶液体积和约为390mL,它们的浓度均小于6mol/L,再加约110mL18 mol/L的浓硫酸,溶质的物质的量为0.24L×1mol/L+0.15L×3mol/L+0.11L×3mol/L=1.02mol,溶液的浓度约为:$\frac{1.02mol}{0.5L}$=2.04mol/L,不能得到6mol/L的500ml硫酸,所以只能选用1000 mL容量瓶,然后根据溶液混合后,溶质的物质的量不变来解答.
解答 解:(1)①、②两溶液体积和约为390mL,它们的浓度均小于6mol/L,再加约110mL18 mol/L的浓硫酸,溶质的物质的量为0.24L×1mol/L+0.15L×3mol/L+0.11L×3mol/L=1.02mol,溶液的浓度约为:$\frac{1.02mol}{0.5L}$=2.04mol/L,不能得到6mol/L的500ml硫酸,所以只能选用1000 mL容量瓶;
故答案为:1000mL;
(2)欲配制6.0mol/L的H2SO4 1 000mL所需硫酸的物质的量:1L×6 mol/L=6mol,由溶液混合前后溶质的物质的量不变,则需要加入的硫酸的物质的量为6mol-0.24L×1mol/L+0.15L×3mol/L=5.31mol,需要浓硫酸的体积V=$\frac{5.31mol}{18mol/L}$=0.295L=295mL;
故答案为:295.0mL.
点评 本题考查了一定物质的量浓度溶液的配制,侧重考查有关物质的量浓度计算,注意容量瓶规格选择方法,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.X、Y、Z、W、R是短周期中的五种元素,其原子序数依次增大,X、W最外层电子数相等,X为地壳中含量最多的元素,Y是短周期中金属性最强的元素,Z单质是生活应用广泛的常见金属单质,下列说法不正确的是( )
| A. | 原子半径:Y>X | B. | 最高价氧化物的水化物的酸性:R>W | ||
| C. | 气态氢化物的稳定性:X>W | D. | 单质与水(或酸)反应的剧烈程度:Z>Y |
10.下表中,对有关除杂的方法不正确的是( )
| 物质 | 杂质 | 方法 | |
| A | 乙烷 | 乙烯 | 一定条件下与H2反应使乙烯转化为乙烷 |
| B | 乙炔 | H2S | 通入CuSO4溶液的洗气瓶洗气 |
| C | 溴苯 | Br2 | 加NaOH溶液后分液 |
| D | 工业酒精 | H2O(转为无水酒精) | 加入生石灰,蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
7.现有部分短周期元素的性质或原子结构如表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是146C,在周期表中的位置是第二周期 IVA族.
(2)元素Y与氢元素形成一种离子YH4+,写出该离子与Z离子形成化合物的电子式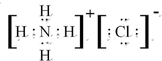 .
.
(3)写出元素X、T形成的化合物XT2的电子式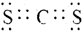 .
.
(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b、d、e(填序号)
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.与铁加热,Z生成三价铁,T生成二价铁
e.T原子与Z原子电子层数相同,Z原子半径小于T原子
(5)T的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为SO2+Cl2+2H2O=2HCl+H2SO4
(6)分别用电子式表示Z与镁元素、Y与氮元素形成化合物的过程: ,
,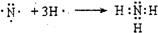 .
.
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数比内层电子总数少4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 与氢形成的气态化合物在标准状况下的密度为0.76g•L-1 |
| Z | 元素最高正价与负价的绝对值之差是6 |
(2)元素Y与氢元素形成一种离子YH4+,写出该离子与Z离子形成化合物的电子式
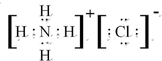 .
.(3)写出元素X、T形成的化合物XT2的电子式
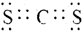 .
.(4)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b、d、e(填序号)
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.与铁加热,Z生成三价铁,T生成二价铁
e.T原子与Z原子电子层数相同,Z原子半径小于T原子
(5)T的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为SO2+Cl2+2H2O=2HCl+H2SO4
(6)分别用电子式表示Z与镁元素、Y与氮元素形成化合物的过程:
 ,
,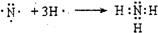 .
.
4.化学与生活密切相关,下列说法不正确的是( )
| A. | “青篙一握,以水二升渍,绞取汁”,该过程是对青篙素的提取,属于化学变化 | |
| B. | 向漂白粉溶液中滴加少量醋酸,漂白速率会加快 | |
| C. | 利用生物方法脱除生活污水中的氮和磷,可防止水体富营养化 | |
| D. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 |
5.某学习研究小根据金属锌、铝、铁分别与稀盐酸反应的相对速率,探究金属锌、铝、铁的金属活动性和反应速率测定.
【实验设计】为了达到实验目的,必须控制实验条件.你认为控制的实验条件是(可填满也可不填满)
(1)反应体系的温度(相同);(2)盐酸的浓度(相同);(3)取用盐酸的体积(相同);(4)金属的(比)表面积(或金属粉末的粗细程度)(相同).
【实验探究】该学习研究小组在上述实验条件相同的情况下,进行三组实验:各量取50mL稀盐酸于小烧杯中,分别同时加入足量的三种表面无氧化膜的金属片,用pH计测定溶液的pH并将信息传输到电脑,电脑动态地绘制出溶液中c(H+)随时间t的变化曲线(反应过程中溶液的体积没有变化).图1是反应到t1s时电脑记录的曲线:
【交流与表达】根据上述c(H+)随时间t的变化曲线回答下列问题: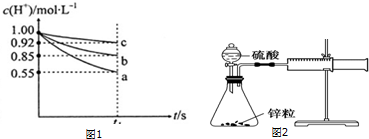
(1)表示金属活动性最弱的金属与H+反应的变化曲线是c(填“a”、“b”或“c”编号).
(2)在同一时间内,表示不同反应的反应速率可以有:同温同压下放出氢气的体积V(H2);溶液中H+浓度的减少△c(H+);固体减少的量△m或△n.在0一t1s之间,设A1和Zn分别与盐酸反应的速率为v(Al)和v(Zn):
Ⅰ.若以溶液中c(H+)减少来表示不同反应的速率,即v(Al):v(Zn)═3:1;
Ⅱ.若以固体质量的减轻来表示不同反应的速率,即v(Al):v(Zn)═54:65;
Ⅲ.若以固体物质的量减少来表示不同反应的速率,即v(Al):v(Zn)═2:1.
IV.可以利用图2所示的装置测定不同浓度的硫酸与锌的反应速率,请回答下列问题:
按照上述装置图安装3套相同的装置,并检验装置气密性良好,将注射器的活栓推至“0”刻度处;然后在三个锥形瓶中分别放入相同形状的锌粒2g,并分别通过分液漏斗在锥形瓶中加入1mol•L-1、2mol•L-1和4mol•L-1的稀硫酸40mL.请补全下表空白:
请选择一组合适的数据填写在第②组实验中的a、b处B.
A.12和0.83B.6和1.67C.1和10D.6和3.67.
【实验设计】为了达到实验目的,必须控制实验条件.你认为控制的实验条件是(可填满也可不填满)
(1)反应体系的温度(相同);(2)盐酸的浓度(相同);(3)取用盐酸的体积(相同);(4)金属的(比)表面积(或金属粉末的粗细程度)(相同).
【实验探究】该学习研究小组在上述实验条件相同的情况下,进行三组实验:各量取50mL稀盐酸于小烧杯中,分别同时加入足量的三种表面无氧化膜的金属片,用pH计测定溶液的pH并将信息传输到电脑,电脑动态地绘制出溶液中c(H+)随时间t的变化曲线(反应过程中溶液的体积没有变化).图1是反应到t1s时电脑记录的曲线:
【交流与表达】根据上述c(H+)随时间t的变化曲线回答下列问题:

(1)表示金属活动性最弱的金属与H+反应的变化曲线是c(填“a”、“b”或“c”编号).
(2)在同一时间内,表示不同反应的反应速率可以有:同温同压下放出氢气的体积V(H2);溶液中H+浓度的减少△c(H+);固体减少的量△m或△n.在0一t1s之间,设A1和Zn分别与盐酸反应的速率为v(Al)和v(Zn):
Ⅰ.若以溶液中c(H+)减少来表示不同反应的速率,即v(Al):v(Zn)═3:1;
Ⅱ.若以固体质量的减轻来表示不同反应的速率,即v(Al):v(Zn)═54:65;
Ⅲ.若以固体物质的量减少来表示不同反应的速率,即v(Al):v(Zn)═2:1.
IV.可以利用图2所示的装置测定不同浓度的硫酸与锌的反应速率,请回答下列问题:
按照上述装置图安装3套相同的装置,并检验装置气密性良好,将注射器的活栓推至“0”刻度处;然后在三个锥形瓶中分别放入相同形状的锌粒2g,并分别通过分液漏斗在锥形瓶中加入1mol•L-1、2mol•L-1和4mol•L-1的稀硫酸40mL.请补全下表空白:
| 序号 | 加入的稀硫酸浓度 | 反应时间/min | 收集的气体/mL | 反应速率mL•min-1 |
| ① | 1mol•L-1 | 11 | 10 | |
| ② | 2mol•L-1 | a | 10 | b |
| ③ | 4mol•L-1 | 10 | 5.0 |
A.12和0.83B.6和1.67C.1和10D.6和3.67.
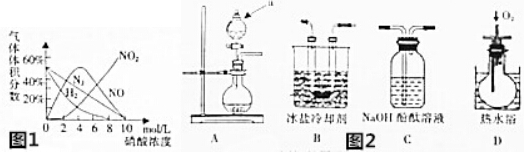
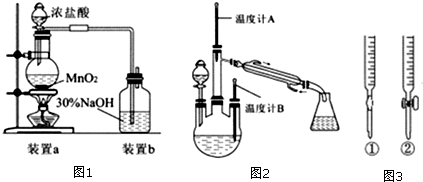
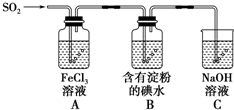 某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示
某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示