题目内容
18.环境保护是当今倍受人们关注的社会问题.下列叙述不正确的是( )| A. | 酸雨能加快桥梁、雕塑的腐蚀 | B. | 煤炭燃烧时,会向空气中排放SO2 | ||
| C. | 向高空排放粉尘,减少空气污染 | D. | 氮氧化物会形成光化学烟雾 |
分析 A.酸雨中含有大量氢离子,能够腐蚀桥梁、雕塑;
B.含有硫的煤炭燃烧时会排放出污染空气的有毒气体SO2;
C.粉尘仍然会排放,无法减少空气污染;
D.光化学烟雾的形成主要是汽车尾气排放出的氮氧化物发生复杂的变化造成的.
解答 解:A.酸雨的pH小于5.6,具有较强腐蚀性,能够加快桥梁、雕塑的腐蚀,故A正确;
B.煤炭中含有S元素,则煤炭燃烧时会向空气中排放SO2,故B正确;
C.向高空排放粉尘,粉尘仍然会排放,没有减少空气污染,故C错误;
D.光化学烟雾的罪魁祸首为氮的氧化物,故D正确;
故选C.
点评 本题考查环境污染及治理,题目难度不大,明确常见环境污染类型、成因及治理措施为解答关键,试题侧重基础知识的考查,有利于提高学生的环保意识.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
8.下列指定反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向NaAlO2溶液通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
9.设NA为阿伏伽德罗常数的值,下列叙述正确的为( )
| A. | 密闭容器中2molNO 和 1molO2 充分反应,产物的分子数为2NA | |
| B. | 常温下,1L0.1mol/LnaCO3 溶液中含有的离子总数为0.3 NA | |
| C. | 0.1mol铁在0.1molCl2 中充分燃烧,转移的电子数为0.3 NA | |
| D. | 标况下,1.12L16O2 和1.12L18O2 均含有 0.1 NA个氧原子 |
6.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA | |
| B. | 常温常压下,28 g C2H4、CO的混合气体中含有碳原子的数目为1.5NA | |
| C. | 1mol Na2O2 固体中含阴阳离子的数目为3NA | |
| D. | 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
10.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 L酒精含有的分子数为NA | |
| B. | 500mL lmoL/L的盐酸中含有的HC1分子数为0.5 NA | |
| C. | 2.24LH2含有0.2NA个氢原子 | |
| D. | 通常状况下,71 g Cl2所含原子数为2NA |
7.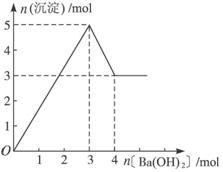 如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
 如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )
如图表示在某溶液中滴加Ba(OH) 2溶液时,沉淀的物质的量随Ba(OH) 2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO 4 | B. | Al 2(SO 4) 3 | C. | Fe 2(SO 4) 3 | D. | NaAlO 2 |
7.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol羟基含10 NA个电子 | |
| B. | 标准状况下,11.2L四氯化碳所含分子总数为0.5NA | |
| C. | 1 mol聚乙烯含有的原子总数目为6NA | |
| D. | 20℃时,2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |