题目内容
物质的量浓度相同的下列溶液中,NH4+浓度最小的是( )
| A、NH4Cl |
| B、NH4HSO4 |
| C、CH3COONH4 |
| D、NH3?H2O |
考点:盐类水解的原理,弱电解质在水溶液中的电离平衡
专题:盐类的水解专题
分析:根据铵根离子的浓度和水解的影响角度来分析,如果含有对铵根离子水解起促进作用的离子,则铵根离子水解程度增大,如果含有抑制铵根离子水解的离子,则铵根的水解程度减弱.
解答:
解:物质的量浓度相同的下列溶液中不考虑(水解)其他因素影响,ABC选项中铵根离子浓度分别比为1:1:1,D中NH3?H2O部分电离;
A、氯化铵中,铵根离子的水解不受氯离子的影响;
B、硫酸氢铵中的氢离子对铵根的水解起抑制作用,导致铵根离子水解程度较小,铵根离子浓度较大;
C、醋酸根离子对铵根离子的水解起到促进作用,导致铵根离子水解程度大,其铵根离子浓度较小;
D、NH3?H2O是弱电解质,部分电离,其铵根离子浓度最小;
故选D.
A、氯化铵中,铵根离子的水解不受氯离子的影响;
B、硫酸氢铵中的氢离子对铵根的水解起抑制作用,导致铵根离子水解程度较小,铵根离子浓度较大;
C、醋酸根离子对铵根离子的水解起到促进作用,导致铵根离子水解程度大,其铵根离子浓度较小;
D、NH3?H2O是弱电解质,部分电离,其铵根离子浓度最小;
故选D.
点评:本题考查学生离子的水解的影响因素、弱电解质的电离,注意把握影响盐的水解的因素,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
部分弱酸的电离平衡常数如表,下列说法不正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、CN-+H2O+CO2═HCN+HCO3- |
| B、中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
| C、c (NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液,物质的量浓度大小顺序为:c (NH4HCO3)>c (NH4CN)>c (HCOONH4) |
| D、pH=8.3的NaHCO3溶液:c (Na+)>c (HCO3- )>c (H2CO3)>c (CO32- ) |
科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、该电池反应中MnO2起催化作用 |
| B、该电池的正极反应为:MnO2-e-+H2O═MnO(OH)+OH- |
| C、导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D、电池工作时,负极周围溶液的pH将不断变大 |
下列说法中错误的是( )
| A、许多化学反应中的能量变化表现为热量的放出和吸收 |
| B、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C、无需加热的反应一定是放热反应 |
| D、恒温、恒压条件下的反应热叫做焓变 |
 如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )
如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )| A、升高温度 |
| B、迅速缩小容器体积 |
| C、增大X的浓度 |
| D、增大Y的浓度 |
23g金属钠(发生反应2Na+2H2O=2NaOH+H2↑)溶于多少克水中,可使所得溶液中Na+与水分子个数之比为1:10( )
| A、18g | B、180g |
| C、198g | D、162g |
用惰性电极电解下列溶液一段时间后,再加入一定量的某种纯净物(括号内物质),不能使溶液恢复到原来的成分和浓度的是( )
| A、KCl(HCl) |
| B、H2SO4(H2O) |
| C、AgNO3(HNO3) |
| D、CuSO4(CuCO3) |
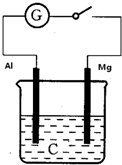 如图所示,把电极Al、Mg插入C的溶液中设计原电池.
如图所示,把电极Al、Mg插入C的溶液中设计原电池.