题目内容
1.近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下: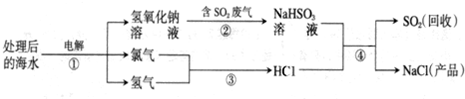
(1)上图中从海水最终得到“NaCl(产品)”的过程属于化学变化(填“物理变化”或“化学变化”).
(2)图中反应①、③、④属于化合反应的是③ (填序号).
(3)①中的反应物是氯化钠和,该反应的化学方程式为2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;.
(4)反应④的化学方程式为NaHSO3+HCl═NaCl+H2O+SO2↑.
分析 处理后的海水电解得到氢氧化钠溶液、氯气、氢气,氢气和氯气反应生成氯化氢溶于水形成盐酸,含二氧化硫的废气通入氢氧化钠溶液得到亚硫酸氢钠溶液,和盐酸反应生成二氧化硫和氯化钠,
(1)分析过程可知获得氯化钠的过程中发化学反应;
(2)两种或两种以上物质反应生成一种物质的反应为化合反应;
(3)电解氯化钠溶液生成氢氧化钠、氯气和水;
(4)反应④是亚硫酸钠和盐酸反应生成氯化钠、水和二氧化硫.
解答 解:(1)从海水最终得到“NaCl(产品)”是反应生成的氯化钠,该变化属于化学变化,
故答案为:化学变化;
(2)氯气和氢气反应生成氯化氢的反应属于化合反应,
故答案为:③;
(3)①中的反应物是氯化钠和水,电解氯化钠溶液生成氢氧化钠、氯气和水,反应的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:水:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)反应④是亚硫酸钠和盐酸反应生成氯化钠、水和二氧化硫,反应的化学方程式为:NaHSO3+HCl═NaCl+H2O+SO2↑,
故答案为:NaHSO3+HCl═NaCl+H2O+SO2↑.
点评 本题主要考查了化学方程式的书写及其物质变化的分类等方面的内容,主要是过程分析判断,物质性质和实验操作是解题关键,题目难度不大.

练习册系列答案
相关题目
11.下列变化过程中,没有破坏化学键的是( )
| A. | 氯化钠的融化 | B. | 乙醇溶于水 | C. | 乙烯的燃烧 | D. | 水的通电分解 |
12.下列关于碱金属的叙述,正确的是( )
| A. | 金属钠着火时,可用水或泡沫灭火器灭火 | |
| B. | 碱金属单质都可保存在煤油中 | |
| C. | 钠离子半径比钠原子半径小 | |
| D. | 碱金属中密度最小,熔、沸点最高的是铯 |
9.下列属于化学变化的是( )
| A. | 向饱和的硫酸铵溶液中滴加蛋清溶液 | |
| B. | 日本核电站工作人员给核电机组注水降温 | |
| C. | 炼油厂蒸馏原油获得汽油、煤油等产品 | |
| D. | 露置于空气中的镁带表面逐渐变黑 |
6.下列反应的离子方程式正确的是( )
| A. | 向AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═A1O2-+4NH4++2H2O | |
| B. | NaHCO3溶液和足量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| C. | 酸性条件下,KIO3溶液与KI溶液反应:IO3-+5I-+3H2O═3I2+6OH- | |
| D. | Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+═2Fe3++2H2O |
6.下列物质互为同分异构体的一组是( )
| A. | 甲醇和乙醇 | B. | 丁烷和异丁烷 | C. | 20Ne和22Ne | D. | 金刚石和石墨 |
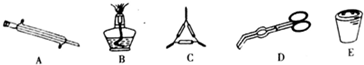
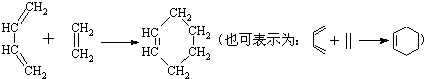
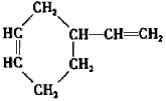 .
.