题目内容
3.下列说法不正确的是( )| A. | 铁盐比铝盐更适合做净水剂 | B. | 光导纤维的主要成分是二氧化硅 | ||
| C. | 氧化镁可以做耐火材料 | D. | 合金一定比纯金属耐腐蚀 |
分析 A.铁盐是高铁酸钾具有氧化性可以杀菌消毒,被还原的产物铁离子解程度比铝盐水解程度大,更易形成胶体;
B.二氧化硅具有良好的光学特性;
C.耐火材料应具有较高的熔点;
D.在潮湿空气中两种金属各部分接触会与空气中的水共同作用形成一个个微型的原电池.
解答 解:A.铝盐是铝离子水解生成氢氧化铝胶体,胶体可以吸附水中的杂质,铁净水指的是高铁酸钠的强氧化性可以杀菌,被还原为铁离子后可以形成的Fe(OH)3胶体也和Al(OH)3胶体一样可以吸附杂质,铁盐比铝盐更适合做净水剂,故A正确;
B.二氧化硅具有良好的光学特性,是制造光导纤维主要原料,故B正确;
C.氧化镁熔点高,可以做耐火材料,故C正确;
D.在潮湿空气中两种金属各部分接触会与空气中的水共同作用形成一个个微型的原电池,从而引发电子转移促使化学反应的发生程度加剧,纯铁不易被腐蚀,而生铁易被腐蚀,故D错误;
故选D.
点评 本题考查盐类水解的分析应用,二氧化硅、氧化镁的用途,熟练掌握物质的组成和性质,主要合金性质的分析判断是解题关键,题目难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
13.已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②产生 刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是( )
| A. | 反应中硫酸作氧化剂 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 1mol NH4CuSO3完全反应转移0.05mol电子 | |
| D. | 刺激性气味的气体是SO2气体 |
11.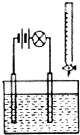 对电解质溶液的导电性进行实验,其装置如图所示.若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗至熄灭,后又逐渐变亮的是( )
对电解质溶液的导电性进行实验,其装置如图所示.若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗至熄灭,后又逐渐变亮的是( )
 对电解质溶液的导电性进行实验,其装置如图所示.若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗至熄灭,后又逐渐变亮的是( )
对电解质溶液的导电性进行实验,其装置如图所示.若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗至熄灭,后又逐渐变亮的是( )| A. | 盐酸中逐滴加入NaCl溶液 | B. | 氢硫酸中逐滴加入氢氧化钠溶液 | ||
| C. | 醋酸中逐滴加氨水 | D. | 硫酸中逐滴加入氢氧化钡溶液 |
18.下列实验操作正确且从安全角度考虑的是( )
①点燃乙炔前,应先检验乙炔纯度
②处理含氨气的尾气,可将导管直接通入盛稀盐酸的烧杯里
③给烧瓶中的液体加热时应加入碎瓷片
④在氯化氢气体中灼烧氯化镁晶体制得无水氯化镁
⑤配制酒精与浓硫酸混合液:先向烧杯里注入酒精,后注入浓硫酸,并不断搅拌
⑥为了便于观察,将钠块放入装有水的试管里反应,并塞紧塞子.
①点燃乙炔前,应先检验乙炔纯度
②处理含氨气的尾气,可将导管直接通入盛稀盐酸的烧杯里
③给烧瓶中的液体加热时应加入碎瓷片
④在氯化氢气体中灼烧氯化镁晶体制得无水氯化镁
⑤配制酒精与浓硫酸混合液:先向烧杯里注入酒精,后注入浓硫酸,并不断搅拌
⑥为了便于观察,将钠块放入装有水的试管里反应,并塞紧塞子.
| A. | ①②④ | B. | ①③⑤ | C. | ③④⑥ | D. | ③⑤⑥ |
12.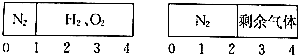 在一个密闭容器中用一可移动板隔开,左边充有氮气,右边充入H2、O2,在室温下用电火花点燃混合气体,反应后仍冷却至室温,隔板终止于容器中点,则原混合气体中H2、O2的体积比是( )
在一个密闭容器中用一可移动板隔开,左边充有氮气,右边充入H2、O2,在室温下用电火花点燃混合气体,反应后仍冷却至室温,隔板终止于容器中点,则原混合气体中H2、O2的体积比是( )
 在一个密闭容器中用一可移动板隔开,左边充有氮气,右边充入H2、O2,在室温下用电火花点燃混合气体,反应后仍冷却至室温,隔板终止于容器中点,则原混合气体中H2、O2的体积比是( )
在一个密闭容器中用一可移动板隔开,左边充有氮气,右边充入H2、O2,在室温下用电火花点燃混合气体,反应后仍冷却至室温,隔板终止于容器中点,则原混合气体中H2、O2的体积比是( )| A. | 2:7 | B. | 6:3 | C. | 4:5 | D. | 8:1 |
13.设NA代表阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 0.1NA个H2分子的质量为0.2g | |
| B. | 常温常压下,11.2L氯气所含的原子数目为NA | |
| C. | 32g氧气的体积为22.4L | |
| D. | 体积相同的H2和O2含有相同的分子数 |
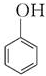 +nHCHO$\stackrel{H+}{→}$
+nHCHO$\stackrel{H+}{→}$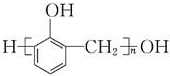 +(2n-1)H2O
+(2n-1)H2O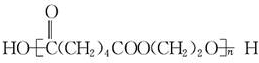 +(2n-1)H2O
+(2n-1)H2O .
.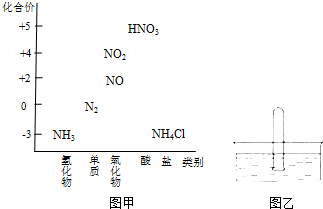 图甲为氮及其化合物的类别与化合价对应的关系图.
图甲为氮及其化合物的类别与化合价对应的关系图.