题目内容
14.Fe(OH)2在空气中被O2反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3.分析 Fe(OH)2中的铁为+2价的铁,很不稳定,露置在空气中容易被氧化成+3价的铁,氧气为氧化剂,根据得失电子守恒和原子守恒书写.
解答 解:+2价的铁易被氧气氧化成+3价的铁,Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(+2→+3)失去1个电子,O2(0→-2)得到4个电子,所以含铁物质前的系数为4,根据根据得失电子守恒和原子守恒发生反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查方程式的书写,掌握铁的化合物的性质是解答的关键,题目较简单.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
2.下列反应属于氧化还原反应的是( )
| A. | NaOH+HCl=NaCl+H2O | B. | Fe+2HCl=FeCl2+H2↑ | ||
| C. | 2NaOH+CO2=Na2CO3+H2O |
19.在铁的吸氧腐蚀中,发生还原反应的那个电极上进行的电极反应是( )
| A. | 2H2O+O2+4e-=4OH- | B. | 2H++2 e-=H2↑ | ||
| C. | 4H++O2+4e-=2H2O | D. | Fe-2 e-=Fe2+ |
3.下列说法不正确的是( )
| A. | 铁盐比铝盐更适合做净水剂 | B. | 光导纤维的主要成分是二氧化硅 | ||
| C. | 氧化镁可以做耐火材料 | D. | 合金一定比纯金属耐腐蚀 |
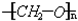 ,是通过加聚反应制得的,合成人造象牙的单体是HCHO
,是通过加聚反应制得的,合成人造象牙的单体是HCHO