题目内容
4.下列有关化学键与晶体结构说法正确的是( )| A. | 两种元素组成的分子一定只有极性键 | |
| B. | 非金属元素组成的化合物一定是共价化合物 | |
| C. | 对于组成结构相似的分子晶体,相对分子质量越大,熔沸点一定越高 | |
| D. | 含阴离子的化合物一定有阳离子 |
分析 A、两种元素组成的分子一定含有极性键,可能含有非极性键;
B、共价化合物中只含共价键,非金属元素组成的化合物不一定是共价化合物;
C、组成结构相似的分子晶体,相对分子质量越大,熔沸点一定越高,但含有氢键的化合物异常;
D、含有阴离子的化合物一定含有阳离子,含有阳离子的物质不一定含有阴离子.
解答 解:A、烃是由两种元素组成的化合物,不仅含有极性键还含有非极性键,故A错误;
B、NH4Cl全部是由非金属元素组成的,但氯化铵是离子化合物,故B错误;
C、如卤族元素的氢化物中,氯、溴、碘的氢化物随着相对分子质量的增其熔沸点逐渐增大,但氟化氢中含有氢键导致其熔沸点较大,故C错误;
D、离子化合物中阴阳离子所带电荷相等,所以含有阳离子的化合物一定含有阴离子,故D正确;
故选D.
点评 本题考查了化学键与晶体的关系,明确氢键的存在导致物质熔沸点改变,知道含有金属阳离子的物质不一定含有阴离子,如金属单质.

练习册系列答案
相关题目
13.下列关于溶液的配制说法不正确的是( )
| A. | 将质量分数为98%的浓硫酸稀释成质量分数为20%的稀硫酸要用容量瓶配制 | |
| B. | 配制100mL1mol/L的氢氧化钠溶液,称量固体质量为4.0g | |
| C. | 容量瓶在定容时,若视线仰视,会使得配制出的溶液物质的量浓度偏小 | |
| D. | 容量瓶洗涤时,若瓶底上有少量蒸馏水,可不必烘干直接使用 |
15.下列说法中不正确的是( )
①高分子化合物不溶于任何溶剂
②高分子化合物对环境都会产生污染
③天然高分子材料主要成分都是纤维素
④塑料均有热塑性
⑤许多合成高分子材料在性能上优于天然高分子材料.
①高分子化合物不溶于任何溶剂
②高分子化合物对环境都会产生污染
③天然高分子材料主要成分都是纤维素
④塑料均有热塑性
⑤许多合成高分子材料在性能上优于天然高分子材料.
| A. | ①③④⑤ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②③④ |
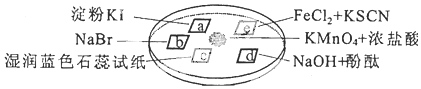
12.如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O
对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
| A. | A | B. | B | C. | C | D. | D |
19.对于 CH3-C≡C-CH3分子,下列说法正确的是( )
| A. | 四个碳原子不可能在一条直线上 | B. | 所有原子在同一平面内 | ||
| C. | 在同一直线上的原子最多为4个 | D. | 在同一直线上的原子最多为6个 |
9.下列四组离子中一定能大量共存的是( )
| A. | K+、H+、Cl-、CO32- | B. | Fe3+、Mg2+、NO3-、SCN- | ||
| C. | NO3- H+、Fe2+、SO42- | D. | Na+、OH-、Cl-、NO3- |
13.在实验室里,要想使AlCl3溶液中的 Al的全部沉淀出来,应选用下列试剂中.( )
| A. | 石灰水 | B. | NaOH 溶液 | C. | 硫酸 | D. | 氨水 |