题目内容
4.取少量 Fe2O3粉末( 红棕色) 加入适量盐酸,得到黄色溶液,用此溶液进行以下实验:(1)在小烧杯中加入20mL 蒸馏水,加热至沸腾后,向沸水中加入制取的黄色溶液 2mL,继续煮沸至液体呈红褐色,停止加热,用激光笔照射烧杯中的液体,可以观察到液体中丁达尔效应,用这个实验可以区别胶体和溶液.
(2)向烧杯中逐滴加入过量的盐酸,会出现一系列变化:现象先出现红褐色沉淀,然后沉淀溶解;原因氢氧化铁胶体遇电解质聚沉,然后与盐酸反应沉淀溶解,Fe(OH)3+3H+=Fe3++3H2O( 用离子方程式表示)
分析 (1)根据制取胶体的实验分析;氢氧化铁胶体具有丁达尔效应,溶液没有丁达尔效应;
(2)氢氧化铁胶体胶体遇到盐酸(电解质溶液)会发生聚沉;氢氧化铁沉淀,继续加入盐酸,会发生酸碱中和反应.
解答 解:(1)向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变成红褐色,即可制得氢氧化铁胶体,反应为Fe3++3H2O?Fe(OH)3(胶体)+3H+,胶体中分散质粒子直径在1nm~100nm之间,用激光笔照射烧杯中的液体,从入射光的垂直方向可以观察到液体中出现的一条光亮的“通路”,这就是丁达尔效应,氢氧化铁胶体具有丁达尔效应,溶液没有丁达尔效应,可以用丁达尔效应来区分胶体和溶液,
故答案为:红褐;丁达尔效应;胶体、溶液;
(2)能使胶体聚沉的方法有:加入带相反电荷胶粒的胶体、加热、加入电解质溶液.氢氧化铁胶体胶体遇到盐酸(电解质溶液)会发生聚沉,产生红褐色氢氧化铁沉淀,氢氧化铁胶体聚沉后会产生氢氧化铁沉淀,继续加入盐酸,会发生酸碱中和反应,生成氯化铁和水,离子方程式为Fe(OH)3+3H+=Fe3++3H2O,
故答案为:先出现红褐色沉淀,然后沉淀溶解;氢氧化铁胶体遇电解质聚沉,然后与盐酸反应沉淀溶解,Fe(OH)3+3H+=Fe3++3H2O.
点评 本题考查胶体中胶体粒子的直径及胶体的性质,注意丁达尔效应是胶体特有的性质、掌握胶体的制备是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.根据:2Fe3++2I-=2Fe2++I2;Br2+2Fe2+=2Fe3++2Br-两个反应,判断Fe3+、I2、Br2的氧化性顺序为( )
| A. | I2>Fe3+>Br2 | B. | Br2>I2>Fe3+ | C. | Br2>Fe3+>I2 | D. | Fe3+>Br2>I2 |
15.V L Fe2(SO4)3溶液中含Fe3+ x mol,溶液中的物质的量浓度是( )
| A. | $\frac{x}{V}$mol/L | B. | $\frac{x}{2V}$mol/L | C. | $\frac{3x}{V}$mol/L | D. | $\frac{3x}{2V}$mol/L |
19.古诗词是古人为我们留下的宝贵精神财富. 下列诗句中不涉及氧化还原反应的是( )
| A. | 野火烧不尽,春风吹又生 | B. | 爆竹声中一岁除,春风送暖入屠苏 | ||
| C. | 春蚕到死丝方尽,蜡炬成灰泪始干 | D. | 粉身碎骨浑不怕,要留清白在人间 |
9.A、B、C、D、E五种短周期主族元素,原子序数依次增大,其中A元素的某种原子无中子,D2-与E+电子层结构相同,B的最外层电子数是电子层数的两倍.下列说法正确的是( )
| A. | 原子半径:E>D>C>B>A | |
| B. | B、C、D与A形成的化合物中,D的化合物沸点一定最高 | |
| C. | A与B、C、D、E形成的化合物中A的化合价均为+1价 | |
| D. | A、B、C、D四种元素形成的某种离子化合物与酸和碱反应都可能放出气体 |
16.某反应过程能量变化如图所示,下列说法正确的是( )
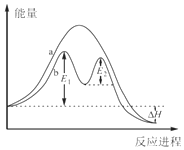

| A. | 反应过程a有催化剂参与 | |
| B. | 该反应为吸热反应,热效应等于△H | |
| C. | 有催化剂的条件下,反应的活化能等于E1+E2 | |
| D. | 改变催化剂,可改变该反应的活化能 |