题目内容
5.工业生产高纯硅涉及的化学方程之一为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,该反应属于( )| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
分析 SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑为单质与化合物反应生成新单质、化合物的反应,以此来解答.
解答 解:A.SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑为单质与化合物反应生成新单质、化合物的反应,属于置换反应,故A选;
B.反应物有两种,不是分解反应,故B不选;
C.生成物有两种,不是化合反应,故C不选;
D.反应物、生成物均有单质,不是复分解反应,故D不选;
故选A.
点评 本题考查二氧化硅的性质及反应类型,为高频考点,把握反应的特点、物质及反应的分类为解答的关键,注意基本反应类型的判断,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
16.某兴趣小组同学利用如图装置测定铁矿石样品的含量.
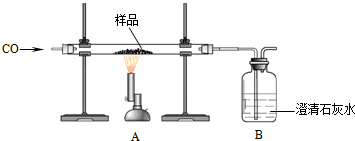
(1)A中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,B中的实验现象是澄清石灰水变浑浊.
(2)待充分反应后,该小组同学记录的实验数据如下:
兴趣小组同学经过讨论后认为不能选用的数据是(“装置A”或“装置B”),其理由是装置B不能将反应产生的CO2全部吸收.该铁矿石中含有氧化铁的质量分数为64%.

(1)A中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,B中的实验现象是澄清石灰水变浑浊.
(2)待充分反应后,该小组同学记录的实验数据如下:
| 样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
| 2.50g | 反应前55.56g | 反应前281.00g |
| 反应后55.08g | 反应后281.25g |
13.下列除去杂质的方法不正确的是( )
| A. | 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 加入新制的生石灰,再加热蒸馏,可以除去乙醇中的少量水 | |
| D. | Mg(OH)2中混有少量Al(OH)3,加入足量烧碱溶液,充分反应,过滤 |
20.科学家研究发现${\;}_{82}^{212}$Pb具有杀死癌细胞的功效.下列关于${\;}_{82}^{212}$Pb的说法正确的是( )
| A. | 质子数是212 | B. | 中子数是130 | C. | 电子数是194 | D. | 质量数是82 |
10.我国古代的有关典籍中有“银针验毒”的记载,“银针验毒”的反应原理之一是4Ag+2H2S+O2═2Ag2S+2H2O.下列有关该反应的说法正确的是( )
| A. | O2被还原 | B. | Ag是氧化剂 | C. | Ag得到电子 | D. | O2发生氧化反应 |
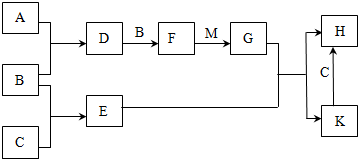
 .
.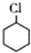 (一氯环己烷)$→_{II}^{NaOH,乙醇,△}$
(一氯环己烷)$→_{II}^{NaOH,乙醇,△}$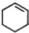 $→_{Ⅲ}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{Ⅳ}{→}$
$→_{Ⅲ}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{Ⅳ}{→}$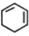

 .
.