��Ŀ����
7���̶�������CO2����Ч��������Դ�������ٿ����е��������壮ij�߷��ӻ�����F�������з�Ӧ�Ƶã�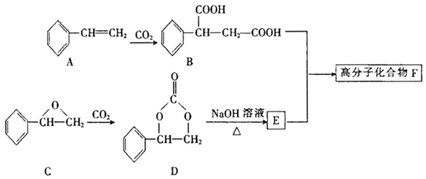
��1��A������Ϊ����ϩ
��2��E�й����ŵ�����Ϊ�ǻ�����AҲ������ȡE���䷢����Ӧ�ķ�Ӧ��������Ϊ�ӳɷ�Ӧ��ȡ����Ӧ
��3���{���ӻ�����F�Ľṹ��ʽΪ
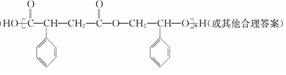
��4��G��C��һ��ͬ���칹�壬������к�һ�������������ϵ�һ�ȴ��������֣����ܷ���������Ӧ����G�Ľṹ��ʽΪ
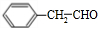 ��G�����Ƶ�Cu��OH��2����Һ��ϼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ
��G�����Ƶ�Cu��OH��2����Һ��ϼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ
��5�����й����л���D��E��˵���У���ȷ����AD
A��D��������������ڷ����廯����
B��D���������е���ԭ���п�����ͬһƽ����
C��E�ĺ˴Ź���������4�����շ�
D��E�ܷ����ӳɷ�Ӧ��ȡ����Ӧ����ȥ��Ӧ��
���� A�����ӳɷ�Ӧ����B��C�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��B��E������Ӧ���ɸ߷��ӻ����B�к��������Ȼ�����D�к����������ǻ���EΪ ��B+E��F����FΪ
��B+E��F����FΪ �������Ŀ�������
�������Ŀ�������
��� �⣺A�����ӳɷ�Ӧ����B��C�����ӳɷ�Ӧ����D��D����ˮ�ⷴӦ����E��B��E������Ӧ���ɸ߷��ӻ����B�к��������Ȼ�����D�к����������ǻ���EΪ ��B+E��F����FΪ
��B+E��F����FΪ ��
��
��1������A�Ľṹ��ʽ֪��A������Ϊ����ϩ���ʴ�Ϊ������ϩ��
��2��EΪ ��E�й������������ǻ���A�ȷ����ӳɷ�Ӧ����±����Ȼ��±��������ˮ�ⷴӦ����E�����Է����ķ�Ӧ����Ϊ�ӳɷ�Ӧ��ȡ����Ӧ��
��E�й������������ǻ���A�ȷ����ӳɷ�Ӧ����±����Ȼ��±��������ˮ�ⷴӦ����E�����Է����ķ�Ӧ����Ϊ�ӳɷ�Ӧ��ȡ����Ӧ��
�ʴ�Ϊ���ǻ����ӳɷ�Ӧ��ȡ����Ӧ��
��3��ͨ�����Ϸ���֪��F�ṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4��G��C��һ��ͬ���칹�壬������к�һ�������������ϵ�һ�ȴ��������֣����ܷ���������Ӧ����G�Ľṹ��ʽΪ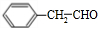 ��G�����Ƶ�Cu��OH��2����Һ��ϼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ
��G�����Ƶ�Cu��OH��2����Һ��ϼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ��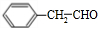 ��
�� ��
��
��5��A���������е���ԭ�ӱ�����ԭ�ӻ���ԭ������ȡ�������ɵ�һϵ�л������Ϊ���������A��D��������������б�����Ҳ���ڷ����廯�����A��ȷ��
B������D�Ľṹ��ʽ��֪��D��������CΪ���ͽṹ��������������ԭ�ӹ��棬��B����
C��E�������ֲ�ͬ�⣬����˴Ź���������6���壬��C����
D��E�к��б������ܷ����ӳɷ�Ӧ�������ǻ����ܷ���ȡ����Ӧ��ˮ�ⷴӦ������ȥ��Ӧ����D��ȷ��
��ѡAD��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶϼ��ۺ�֪ʶ���������������ȷ�л���ṹ�����ʹ�ϵ������֮���ת���ǽⱾ��ؼ���ע��D�к�������Ϊ̼���������Ϊ�״��㣮

 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�| A�� | 1mol��������ȫȼ��ʱ���ų����������������ʵ�ȼ���� | |
| B�� | �����κλ�ѧ��Ӧ����Ӧ������Խ��Ӧ����Խ���� | |
| C�� | SO2����ˮ�ܵ��磬����SO2�ǵ���� | |
| D�� | ij��Һ��pH=7�������Һ��һ��Ϊ���� |
| A�� | 0.1mol��OH-�к��еĵ�����Ϊ0.9NA | |
| B�� | ��״���£�11.2 L CCl4����������Ϊ0.5NA | |
| C�� | 6.02��1022�� CH4������ԭ����Ϊ0.4NA | |
| D�� | ���³�ѹ�£�28 g N2������ԭ�Ӹ���ΪNA |
| A�� | ����ʽΪC7H8O�Һ��������л���������4�� | |
| B�� | �Ҵ���ʹ���Ը��������Һ��ɫ | |
| C�� | �������ˮ���Ʊ������ɱ�ϩ��ˮ��Ӧ�Ʊ�����Ӧ������ͬ | |
| D�� |  ��FeCl3��Һ������ɫ ��FeCl3��Һ������ɫ |
ʵ��1����һ�ݼ����������ռ���ȣ������������ڱ�״����Ϊ224mL��
ʵ��2���ڶ����ȼ������������ᣬ�������ټ���������BaCl2��Һ���ù���2.33g��
����˵����ȷ���ǣ�������
| A�� | ����Һ�п��ܺ�K+ | |
| B�� | ����Һ�п϶�����NO3-��SO42-��NH4+��CO32- | |
| C�� | ����Һ��һ������NO3- | |
| D�� | ����Һ��һ����K+����c��K+����0.1mol/L |
| A�� | Fe3+��KSCN��Һ�� | B�� | Cl-��ϡ�����ữ��AgNO3��Һ�� | ||
| C�� | NH4+��NaOH��Һ�� | D�� | SO42-�����ᡢBaCl2��Һ�� |
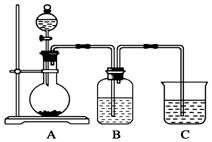 ijͬѧ���ʵ����̽��Ԫ�����ʵĵݱ���ɣ�ʵ��װ����ͼ��ʾ��
ijͬѧ���ʵ����̽��Ԫ�����ʵĵݱ���ɣ�ʵ��װ����ͼ��ʾ��