题目内容
已知:NaCHO3在水溶液中水解的热化学方程式为:NaHCO3(aq)+H2O(l)?H2CO3(aq)+NaOH(aq)△H=+akJ?mol-1;稀盐酸和稀NaOH的中和热为bkJ?mol-1.则等物质的量的NaCHO3与稀盐酸反应的△H等于( )
| A、+(a+b)kJ?mol-1 |
| B、+(a-b)kJ?mol-1 |
| C、-(a-b)kJ?mol-1 |
| D、-(a+b)kJ?mol-1 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:依据盖斯定律结合已知方程式,通过方程式相加减求出目标方程式,再计算反应热.
解答:
解:已知:①NaHCO3(aq)+H2O(l)?H2CO3(aq)+NaOH(aq)△H=+akJ?mol-1,
②HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-bkJ∕mol,
根据盖斯定律:①+②可得,NaHCO3(aq)+HCl(aq)?H2CO3(aq)+NaCl(aq)△H=+(a-b)kJ?mol-1,
故选:B.
②HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=-bkJ∕mol,
根据盖斯定律:①+②可得,NaHCO3(aq)+HCl(aq)?H2CO3(aq)+NaCl(aq)△H=+(a-b)kJ?mol-1,
故选:B.
点评:本题考查了盖斯定律的应用和反应热的计算,侧重于盖斯定律的应用的考查,题目难度中等,注意把握盖斯定律的含义.

练习册系列答案
相关题目
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| B、加入甲基橙试液呈红色的溶液:NH4+,K+,SO42-,Cl- |
| C、Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
| D、pH=12的溶液中:NO3-、I-、Na+、Al3+ |
现有一瓶新制的氯水,将其长时间放置在阳光下,溶液的PH变化正确的是( )

A、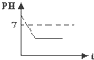 |
B、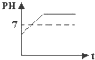 |
C、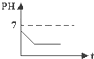 |
D、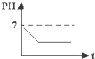 |
下列关于水的说法正确的是( )
| A、我们平时应多饮用很纯净的水,防止有毒物质进入体内 | ||
| B、所有天然水都不能饮用 | ||
C、人体内含有约
| ||
| D、人类可利用的水只占自然界的水极少量,我们应节约用水 |
下列有关环境问题都是由化学物质引起的,在下列组合中对应的化合物不正确的是( )
| A、白色污染:废弃塑料 |
| B、光化学烟雾:二氧化氮? |
| C、臭氧层破坏:氟氯烃? |
| D、温室效应:二氧化硫 |
下列说法不正确的是( )
| A、油脂水解可得到氨基酸和甘油 |
| B、糖类都是溶于水、有甜味的物质 |
| C、所有烷烃都存在碳碳单键 |
| D、所有糖都能水解 |
已知某有机样品3.1g 完全燃烧,燃烧后的混合物通过过量的澄清石灰水,石灰水共增重7.1g,经过滤得10g 沉淀.该有机物的分子式可能是( )
| A、C2H6O2 |
| B、C2H6O |
| C、C2H4O2 |
| D、C2H4O |
空气中的自由电子附着在分子或原子上形成的空气负离子(也叫阴离子)被称为“空气维生素”.O2-就是一种空气负离子,其摩尔质量为( )
| A、32 g |
| B、33 g |
| C、32 g?mol-1 |
| D、33 g?mol-1 |
下列物质的电子式书写正确的是( )
A、N2: |
B、CO2: |
C、Na2O: |
D、HCl: |