题目内容
18.化学与材料、人体健康、环境保护息息相关.丰富多彩的材料为人类的生存和发展创造了完美的物质条件.
(1)金属是一种重要的材料,人类的生活和生产都离不开金属,工业炼铁的主要化学反应方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)石英玻璃的主要成分为二氧化硅,生产陶瓷和硅酸盐水泥所需用到的共同原料是黏土.
(3)有些塑料只是在制造过程中受热时能变软,可以塑制成一定的形状,但加工成型后就不会受热熔化,具有热固性,橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为网状体型结构,从而增大橡胶的强度.
分析 (1)工业上用一氧化碳还原氧化铁炼铁;
(2)石英玻璃的主要成分为二氧化硅,硅酸盐水泥和陶瓷都需用到的共同的主要原料是黏土;
(3)塑料加工成型后就不会受热熔化,具有热固型;天然橡胶通过硫化措施可增大强度和弹性.
解答 解:(1)一氧化碳还原氧化铁生成铁和二氧化碳,方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)石英玻璃的主要成分为二氧化硅,硅酸盐水泥和陶瓷都需用到的共同的主要原料是黏土;
故答案为:二氧化硅;黏土;
(3)塑料加工成型后就不会受热熔化,具有热固型;天然橡胶通过硫化措施使它的分子转化为网状体型结构可增大强度和弹性;
故答案为:热固型;网状体型.
点评 本题为综合题,涉及金属的冶炼、硅酸盐材料的成分、有机高分子材料的性能,题目难度不大,掌握基础是解题关键.

练习册系列答案
相关题目
8.某课题小组研究“铁及其化合物性质”时,向 FeSO4 溶液中滴加少量KSCN溶液,无明显现象.再滴加 H2 O2 溶液时,发现:随着H 2O 2量的增加,溶液先变红,后褪色,并有气泡产生.为弄清楚产生这种异常现象的原因,他们进行了如下探究.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.
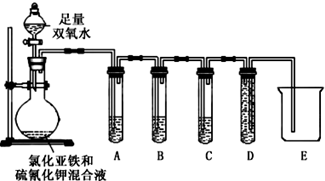
请完成下表中的内容:
[思考与交流]
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.

请完成下表中的内容:
| 实验过程和现象 | 结论 |
| (2)试管A中盛有品红溶液现象:品红溶液褪色 | 证明气体中含有SO2 |
| (3)试管B中现象紫色酸性高锰酸钾溶液颜色不变或变浅试管C中现象:澄清石灰水变浑浊 | 证明气体中含有CO2 |
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
| 实验过程 | 实验现象及结论 |
9.现有三种有机化合物的分子式:①C5H12②C3H6Cl2③C5H10则它们的链状同分异构体数由多到少的顺序为( )
| A. | ③>②>① | B. | ②>①>③ | C. | ①>②>③ | D. | ②>③>① |
13.NO和CO都是汽车尾气力的有害物质,它们能缓慢反应,生成氮气和二氧化碳.为了控制大气污染,对此反应,下列叙述不正确的是( )
| A. | 改变温度对反应速率无影响 | |
| B. | 升高温度能加快反应速率 | |
| C. | 使用催化剂能加快反应速率 | |
| D. | 该反应的化学方程式为:2CO+2NO═N2+2CO2 |
3.某校化学兴趣小组的同学对以下三种品牌牙膏中摩擦剂成分进行调查,结果如下表:
请回答下列问题:
(1)上述三种摩擦剂中属于氧化物的是SiO2(填化学式,下同);
(2)青蛙儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(3)从摩擦剂成分考虑,向佳洁士盐白牙膏样品中滴加少量稀盐酸,可以观察到的现象是有气体生成,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
(4)中华透明牙膏摩擦剂二氧化硅是工业制备晶体硅的原料.工业制备晶体硅的反应原理是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑(用化学反应方程式表示).
| 牙膏品牌 | 青蛙儿童牙膏 | 佳洁士盐白牙膏 | 中华透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂中属于氧化物的是SiO2(填化学式,下同);
(2)青蛙儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(3)从摩擦剂成分考虑,向佳洁士盐白牙膏样品中滴加少量稀盐酸,可以观察到的现象是有气体生成,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
(4)中华透明牙膏摩擦剂二氧化硅是工业制备晶体硅的原料.工业制备晶体硅的反应原理是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑(用化学反应方程式表示).
7.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表所示数据(盐酸的物质的量浓度相等),下列分析推理不正确的是( )
| 盐酸的体积/mL | 50 | 50 | 50 |
| 混合物的质量/g | 9.2 | 15.7 | 27.6 |
| CO2的体积(标准 状况下)/L | 2.24 | 3.36 | 3.36 |
| A. | 盐酸的物质的量浓度为3.0 mol•L-1 | |
| B. | 根据表中数据能计算出混合物中NaHCO3的质量分数为45.65% | |
| C. | 加入混合物9.2 g时盐酸过量 | |
| D. | 15.7 g混合物恰好与盐酸完全反应 |
2.下列有关化学用语表达正确的是( )
| A. | 氨分子的电子式: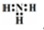 | |
| B. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| C. | O2-的结构示意图为: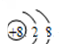 | |
| D. | ${\;}_{35}^{79}$Br的基态原子电子排布式:[Ar]4S24P5 |

