��Ŀ����
��ҵ�ϳ��ú�����Al2O3�ķ�����FeO��V2O5�����۷���ȡV2O5����Ҫ�������£�
��֪���ٱ���ʱAl2O3��V2O5�����봿�Ӧ���������Ӧ�����Σ�ͬʱ�ų�CO2����
�ڳ��������ʵ��ܽ�ȣ�NaVO3��21��2g��l00gˮ��HVO3��0��008g/l00gˮ
��ش𣺣�1����д����������ʱ��V2O5�봿�Ӧ��ѧ����ʽ____ ��
��������B������Ҫ�ɷֿ����Ǣ� ����_ ___ ����_ ___����____ ����д��ѧʽ���ɲ�������
��2�������У���ֱ����H2SO4���ݡ�����A����ȡHVO3��ԭ����____ ��
��3���������١����� ��ϴ�ӡ���������ϴ�ӣ����Ʒ�п��ܺ��еĽ����������� �� ������װ�ã����ּг�����ʡȥ��������ʵ���ҽ��С������ڡ�����____ ��������ţ�
��4��NaVO3����ԭ�͵�����������V2O5������NaOH��Һ����ȡ����Ӧ�����ӷ���ʽΪ____ ��
��1��V2O5 +Na2CO3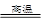 2NaVO3 +CO2 ��2�֣�
2NaVO3 +CO2 ��2�֣�
Fe2O3��Fe3O4������Fe2O3��Fe3O4 ��3�֣�
��2��H2SO4��NaVO3��Ӧ�������ܵ�HVO3��HVO3������һЩ�����ı��棬�谭�˷�Ӧ�Ľ��У��Ӷ�������HVO3���ʣ���ʹ������HVO3���������⣬���������������ᷴӦ���������ӣ����Ӹ������ӣ��������ᣬ�˷���Դ����3�֣�
��3�����ˣ�1�֣�Na+��Al3+��2�֣�B ��2�֣�
��4��V2O5 +2OH�� 2VO3��+ H2O ��2�֣�
2VO3��+ H2O ��2�֣�
���������������1������V2O5���봿�Ӧ���������Ӧ�����Σ�ͬʱ�ų�CO2���壬���仯ѧ����ʽΪV2O5 +Na2CO3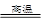 2NaVO3 +CO2���ڱ��յĹ�����FeO������ΪFe2O3��Fe3O4�����ԡ�������B������Ҫ�ɷֿ����Ǣ�Fe2O3��Fe3O4����Fe2O3��Fe3O4
2NaVO3 +CO2���ڱ��յĹ�����FeO������ΪFe2O3��Fe3O4�����ԡ�������B������Ҫ�ɷֿ����Ǣ�Fe2O3��Fe3O4����Fe2O3��Fe3O4
��2����ֱ�Ӽ������ᣬ��A�е����������������ᷴӦ���Ӹ������ӣ��������ᣬ�˷���Դ��ͬʱH2SO4��NaVO3��Ӧ�������ܵ�HVO3��HVO3������һЩ�����ı��棬�谭�˷�Ӧ�Ľ��У��Ӷ�������HVO3���ʣ���ʹ������HVO3������
��3�����������������ܵ�HVO3����������˳������ù�����������ƫ�����Ʒ�Ӧ�������������ӣ���������ϴ�ӳ���������ܺ���Na+��Al3+���������ǰ�HVO3�������ȷֽ��V2O5������Ӧѡ��Bװ�ã�
��4��V2O5������NaOH��Һ�У�����֮һ��NaVO3�������Ʋ���һ������ˮ�����Է�Ӧ�����ӷ���ʽΪ
V2O5 +2OH�� 2VO3��+ H2O
2VO3��+ H2O
���㣺���黯ѧ�л�ѧ����ʽ�����ӷ���ʽ����д����ѧ��Ӧ������жϡ�������ʵ�鲽�衢װ�õ��ж�

����ƹ㷺����ʳƷ��������ʯ�͵ȹ�ҵ�����ϣ�300��400�����ҷֽ⡣��ʵ������ȡ�ķ���֮һ�ǣ�Ca(OH)2 +2HCHO + H2O2 = Ca(HCOO)2 + 2H2O + H2����
ʵ������ȡʱ������ҵ���������ƺͼ�ȩ���μ��뵽��������Ϊ30-70%�Ĺ���������Һ�У�Ͷ�����ʵ���֮������Ϊ1��2��1.2�������տɵõ���������98%�������ؽ����������͵����ʲ�Ʒ��
��1��������������������Զ࣬��Ŀ���� ��
��2����Ӧ�¶���ÿ�����30-70��֮�䣬�¶Ȳ����ߣ�����Ҫԭ���� ��
��3���Ʊ�ʱ�ڻ����Һ��Ҫ���������������Ƽ�ȩ��������Ӧ�⣬��Ҫ����������Na2S��Һ�������Ƶ�Ŀ���� ��
��4��ʵ��ʱ��ǿ������45min����Ŀ���� ���������������Һ��pH 7��8����Ŀ���� ����ᾧ���롢����ò�Ʒ��
��ij�о���ѧϰС���ù�ҵ̼���(��Ҫ�ɷ�ΪCaCO3������Ϊ��Al2O3��FeCO3) Ϊԭ�ϣ����Ʊ������Σ������������Һ�����ȡ����ơ������ͼ�������ʵ��ܽ������������ؽ������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0 mol��L-1����)�����ṩ���Լ��У�a.�����ƣ�b.5mol��L��1���ᣬc. 5mol��L��1���ᣬd. 5mol��L��1���ᣬe. 3%H2O2��Һ��f.����ʯ��ˮ��
�벹��������̼����Ʊ�����Ƶ�ʵ�鲽��
| ���� ���� | ��ʼ���� ��pH | ������ȫ ��pH |
| Fe3�� | 1. 1 | 3. 2 |
| Al3�� | 3. 0 | 5. 0 |
| Fe2�� | 5. 8 | 8. 8 |
����1.��ȡ13.6g����������Լ20mLˮ������ܴ��ã�����ȡ��ϸ��̼�����Ʒ10g���á�
����2. ��
����3. ��
����4.���˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������Ũ���� ��ϴ�ӡ�60��ʱ����ü���ƾ��塣





 �ѳ��ɾ��� ����4��___________________��
�ѳ��ɾ��� ����4��___________________�� 



 CuY2�C+ 2H+����CuSO4��5H2O���������ı���ʽ�� ��
CuY2�C+ 2H+����CuSO4��5H2O���������ı���ʽ�� ��