题目内容
相同质量的两份铝,分别放入足量的等浓度的盐酸和氢氧化钠溶液中,若同温同压下放出相同体积的气体,则消耗的盐酸和氢氧化钠溶液的体积之比为( )
| A、1:1 | B、2:3 |
| C、3:1 | D、3:2 |
考点:化学方程式的有关计算
专题:计算题
分析:铝与足量的氢氧化钠溶液和稀盐酸分别发生2Al+2H2O+2NaOH=2NaAlO2+3H2↑、2Al+6HCl=2AlCl3+3H2↑,若同温同压下放出相同体积的气体,说明铝完全反应,结合反应的方程式计算.
解答:
解:铝与足量的氢氧化钠溶液和稀盐酸分别发生2Al+2H2O+2NaOH=2NaAlO2+3H2↑、2Al+6HCl=2AlCl3+3H2↑,若同温同压下放出相同体积的气体,说明铝完全反应,由方程式可知消耗的氢氧化钠、盐酸的物质的量之比为2:6=1:3,
故选C.
故选C.
点评:本题考查化学方程式的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,明确铝与氢氧化钠的反应方程式及Al的物质的量相同是解题关键,难度中等.

练习册系列答案
相关题目
水中加入下列溶液对水的电离平衡不产生影响的是( )
| A、NaHSO4溶液 |
| B、NaOH溶液 |
| C、KAl(SO4)2溶液 |
| D、KI溶液 |
下列说法中正确的是( )
| A、丙烯分子中有8个σ键,1个π键 |
| B、在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C、NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力 |
| D、NCl3和BC13分子中,中心原子都采用sp3杂化 |
下列离子方程式正确的是( )
| A、氢氧化镁中滴加盐酸:H++OH-═H2O |
| B、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、已知电离平衡常数:H2CO3>HClO>HCO3-,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- |
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2molNa被完全氧化生成1mol Na2O2,得到2NA个电子 |
| B、在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 |
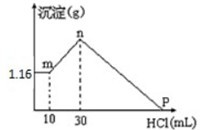 把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示:
把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示: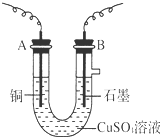 某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)