题目内容
(1)根据如图1所示情况,判断下列说法中正确的是 .

A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=41kJ?mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值大于41kJ?mol-1
(2)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是
(3)如图2是某温度下,N2与H2反应过程中能量变化的曲线图.该反应的热化学方程式为 a、b两条曲线产生区别的原因很可能是 .

A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=41kJ?mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值大于41kJ?mol-1
(2)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是
(3)如图2是某温度下,N2与H2反应过程中能量变化的曲线图.该反应的热化学方程式为
考点:热化学方程式,反应热和焓变
专题:化学平衡专题
分析:(1)据图分析,反应物能量小于生成物,正反应吸热,热化学方程式为:CO2(g)+H2(g)=CO(g)+H2O(g)△H=41kJ?mol-1,水由气态变为液态放热;
(2)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kJ热量,注意标明物质的聚集状态来解答;
(3)该反应放出的能量大于吸收的能量,所以放热,△H=放出的能量-吸收的能量=600kJ/mol-508kJ/mol=92kJ/mol,进而书写热化学方程式;其中曲线b是反应的活化能降低了,反应的焓变不变.
(2)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kJ热量,注意标明物质的聚集状态来解答;
(3)该反应放出的能量大于吸收的能量,所以放热,△H=放出的能量-吸收的能量=600kJ/mol-508kJ/mol=92kJ/mol,进而书写热化学方程式;其中曲线b是反应的活化能降低了,反应的焓变不变.
解答:
解:(1)A、该反应热化学方程式为:CO2(g)+H2(g)=CO(g)+H2O(g)△H=41kJ?mol-1,故A错误;
B、反应物能量小于生成物,正反应吸热,故B正确;
C、正反应吸热,故C错误;
D、水由气态变为液态放热,所以该反应吸热减少,其反应热的值小于41kJ?mol-1,故D错误;
故答案为:B;
(2)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kJ热量,则热化学方程式为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol;
(3)该反应放出的能量大于吸收的能量,所以放热,△H=放出的能量-吸收的能量=600kJ/mol-508kJ/mol=92kJ/mol,该反应的热化学方程式为:N2(s)+3H2(g)=2NH3(g);△H=-92 kJ/mol,其中曲线b是反应的活化能降低了,反应的焓变不变,所以时加入了催化剂所致.
故答案为:N2(s)+3H2(g)?2NH3(g);△H=-92 kJ/mol;a不适用催化剂,b使用了催化剂.
B、反应物能量小于生成物,正反应吸热,故B正确;
C、正反应吸热,故C错误;
D、水由气态变为液态放热,所以该反应吸热减少,其反应热的值小于41kJ?mol-1,故D错误;
故答案为:B;
(2)16g固体硫完全燃烧时放出148.4kJ的热量,即1molS完全燃烧时放出放出296.8kJ热量,则热化学方程式为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-296.8 kJ/mol;
(3)该反应放出的能量大于吸收的能量,所以放热,△H=放出的能量-吸收的能量=600kJ/mol-508kJ/mol=92kJ/mol,该反应的热化学方程式为:N2(s)+3H2(g)=2NH3(g);△H=-92 kJ/mol,其中曲线b是反应的活化能降低了,反应的焓变不变,所以时加入了催化剂所致.
故答案为:N2(s)+3H2(g)?2NH3(g);△H=-92 kJ/mol;a不适用催化剂,b使用了催化剂.
点评:本题考查化学反应中的能量变化及利用盖斯定律确定反应及其能量的关系,注意键能计算焓变的方法,题目难度中等,注重基础知识的考查.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列化学用语书写正确的是( )
A、氯原子的结构示意图: | ||
B、H2O分子的比例模型: | ||
C、作为相对原子质量测定标准的碳核素:
| ||
D、用电子式表示氯化氢分子的形成过程: |
只用一种试剂就能将甘油、苯酚溶液、四氯化碳、己烯、苯五种无色液体分开的是( )
| A、FeCl3溶液 |
| B、NaOH溶液 |
| C、溴水 |
| D、镁 |
纳米是长度单位,1纳米等于1×10-9米,物质的颗粒达到纳米级时,具有特殊的性质.例如将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧.下列对“纳米铜”的有关叙述正确的是( )
| A、常温下“纳米铜”比铜片的还原性强,反应时反应速率快 |
| B、“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快 |
| C、“纳米铜”与铜是同素异形体 |
| D、常温下“纳米铜”比铜片更易得电子,反应时反应速率快 |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH3 实验室用下列方法测定某水样中O2的含量
实验室用下列方法测定某水样中O2的含量 相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题:
相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题: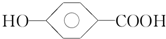 ,该反应的化学方程式是
,该反应的化学方程式是