题目内容
下列化学用语正确的是( )
| A、乙烯分子的最简式:CH2 |
| B、1,2-二溴乙烷的结构简式:C2 H4 Br2 |
| C、羟基的化学式:OH- |
| D、己烷的分子式:C6H12 |
考点:结构简式,分子式
专题:化学用语专题
分析:A、最简式是用元素符号表示化合物分子中各元素的原子个数比的最简关系式;
B、结构简式是指把分子中各原子连接方式表示出来的式子;
C、OH-是氢氧根离子,不是羟基;
D、己烷属于饱和烷烃,分子式为C6H14.
B、结构简式是指把分子中各原子连接方式表示出来的式子;
C、OH-是氢氧根离子,不是羟基;
D、己烷属于饱和烷烃,分子式为C6H14.
解答:
解:A、最简式是用元素符号表示化合物分子中各元素的原子个数比的最简关系式,乙烯分子式为C2H4,故乙烯分子的最简式为CH2,故A正确;
B、结构简式是指把分子中各原子连接方式表示出来的式子,1,2-二溴乙烷的结构简式为 ,故B错误;
,故B错误;
C、OH-是氢氧根离子,羟基化学式为-OH,故C错误;
D、己烷属于饱和烷烃,分子式为C6H14,故D错误;
故选:A.
B、结构简式是指把分子中各原子连接方式表示出来的式子,1,2-二溴乙烷的结构简式为
 ,故B错误;
,故B错误;C、OH-是氢氧根离子,羟基化学式为-OH,故C错误;
D、己烷属于饱和烷烃,分子式为C6H14,故D错误;
故选:A.
点评:本题考查了几种物质和离子的结构简式和分子式的书写,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
SiCl4的分子结构与CH4类似,下列说法中不正确的是( )
| A、SiCl4具有正四面体的构型 |
| B、在SiCl4和CCl4晶体中,前者分子间作用力比后者大 |
| C、常温下SiCl4是气体 |
| D、SiCl4的分子中硅氯键的极性比CCl4中的碳氯键强 |
用价层电子对互斥理论预测CO32-和BF3的立体结构分别是( )
| A、平面三角形;三角锥形 |
| B、三角锥形;平面三角形 |
| C、三角锥形;三角锥形 |
| D、平面三角形;平面三角形 |
以下四种有机物的分子式皆为C4H10O:
①
②CH3CH2CH2CH2OH
③
④
其中既能发生消去反应生成相应的烯烃,又能氧化生成相应醛的是( )
①

②CH3CH2CH2CH2OH
③

④

其中既能发生消去反应生成相应的烯烃,又能氧化生成相应醛的是( )
| A、①② | B、只有② |
| C、②和③ | D、③和④ |
在室温下,pH相同、体积相同的氨水和氢氧化钠溶液,采取下列措施后,有关叙述正确的是( )
| A、温度下降20℃,两溶液的pH均不变 |
| B、各加水稀释10倍,两溶液的pH仍相等 |
| C、分别加入适量的氯化铵晶体,两溶液的pH均减小 |
| D、各用相同物质的量浓度的盐酸中和,所消耗盐酸的体积相等 |
下列叙述中,正确的是( )
| A、12g碳所含的原子数就是阿伏加德罗常数 |
| B、阿伏加德罗常数没有单位 |
| C、“物质的量”指物质的质量 |
| D、摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒 |
合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=-92.4kJ?mol-1.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分为?,下列说法中正确的是
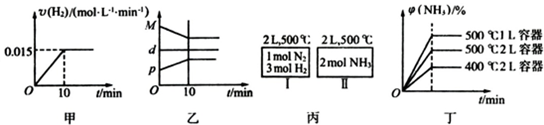 ( )
( )
 ( )
( )| A、若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示 |
| B、反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙 |
| C、如图丙所示,容器I和II达到平衡时所需要的时间可能不同 |
| D、若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示 |
已知某温度、压强下,2molH2的体积是22.4L,下列有关说法中正确的是( )
| A、该条件下,气体的摩尔体积是22.4L?mol-1 |
| B、该条件下,32gO2的体积是22.4L |
| C、该条件下,1molN2的体积是11.2L |
| D、该条件下,9.03×1023个H2O分子的体积是16.8L |
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:

关于咖啡鞣酸的下列叙述正确的是( )

关于咖啡鞣酸的下列叙述正确的是( )
| A、分子式为C16H13O9 |
| B、1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应 |
| C、能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键 |
| D、与浓溴水能发生两种类型的反应 |