题目内容
9.等物质的量的下列物质,与足量氢气发生加成反应,消耗氢气最多的是( )| A. | CH2═CH-CH═CH2 | B. | 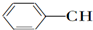 ═CH2 ═CH2 | C. | 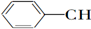 ═CH-CH2 ═CH-CH2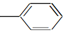 | D. | 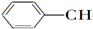 ═CH-CH═ ═CH-CH═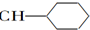 |
分析 苯环、双键、三键均与氢气发生加成反应,苯环与氢气1:3加成,双键与氢气1:1加成,三键与氢气1:2加成,以此计算.
解答 解:设选项中有机物的物质的量均为1mol,则
A.含2个双键,消耗氢气为2mol;
B.含苯环与碳碳双键,消耗氢气为4mol;
C.含2个苯环、1个碳碳双键,消耗氢气为7mol;
D.含1个苯环、2个碳碳双键,消耗氢气为5mol,
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团、有机反应等为解答的关键,侧重分析与应用能力的考查,注意烯烃、苯的性质,题目难度不大.

练习册系列答案
相关题目
20.X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示,已知X、Y、Z的质子数之和为31.试回答:
(1)它们的元素符号是C;Mg;Al.
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
| X | ||
| Y | Z |
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
17.X、Y、Z、W、R属于短周期主族元素.X的原子半径是短周期主族元素中最大的,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1. 下列叙述错误的是( )
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y的氢化物比R的氢化物稳定,熔沸点高 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z | |
| D. | RY2、WY2通入Ba(NO3)2溶液中均无白色沉淀生成 |
4.可逆反应达到平衡的重要特征是( )
| A. | 正、逆反应还在继续进行 | B. | 正、逆反应速率都为零 | ||
| C. | 反应停止 | D. | 正、逆反应速率相等且不为零 |
1.甲烷和乙醇均属于( )
| A. | 酸 | B. | 碱 | C. | 氧化物 | D. | 有机物 |

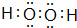 、
、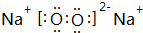 ;
;