题目内容
20.在10L密闭容器中进行2SO2(气)+O2(气)?2SO3(气)反应,10s后SO3增加了4mol,则10s 内SO3的平均反应速率为[单位mol•(L•s)-1]( )| A. | 0.04 | B. | 0.4 | C. | 0.01 | D. | 0.16 |
分析 依据化学反应速率概念计算,10s后SO3增加了4mol,三氧化硫浓度增加=$\frac{4mol}{10L}$=0.4mol/L,依据v=$\frac{△c}{△t}$计算
解答 解:在10L密闭容器中进行2SO2(气)+O2(气)?2SO3(气)反应,三氧化硫浓度增加=$\frac{4mol}{10L}$=0.4mol/L,10s后SO3增加了4mol,
则10s 内SO3的平均反应速率=$\frac{0.4mol/L}{10s}$=0.04mol/(L′s),
故选A.
点评 本题考查化学反应速率有关计算,比较基础,注意概念实质的理解应用,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
10.下列物质中,含有极性键的离子化合物是( )
| A. | CaCl2 | B. | Na2O2 | C. | NaOH | D. | K2S |
11.2015年10月5日,屠呦呦因发现治疗疟疾的青蒿素和双氢青蒿素(结构如图)获得诺贝尔生理学或医学奖.一定条件下青蒿素可以转化为双氢青蒿素.下列有关说法中正确的是( )
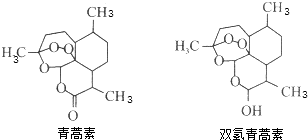

| A. | 青蒿素的分子式为C15H20O5 | |
| B. | 1 mol青蒿素最多能和1 molBr2发生加成反应 | |
| C. | 双氢青蒿素能发生氧化反应、酯化反应 | |
| D. | 青蒿素转化为双氢青蒿素发生了氧化反应 |
8.有机物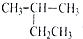 的命名正确的是( )
的命名正确的是( )
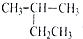 的命名正确的是( )
的命名正确的是( )| A. | 新戊烷 | B. | 异丁烷 | C. | 2-甲基丁烷 | D. | 2-乙基丙烷 |
15.分子式为C5H10的烃与H2O反应后的产物中,能与金属Na反应放出气体的有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
5.下列烃中能生成四种一氯代物的是( )
| A. | (CH3)2CHCH2CH2CH3 | B. |  | C. | 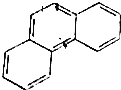 | D. | (CH3)3CCH2CH3 |
12.在自然界存在游离态的元素是( )
| A. | 硫 | B. | 氯 | C. | 铝 | D. | 镁 |
9.如表是元素周期表的一部分,回答下列问题:
(1)在这些元素中,F(用元素符号填写,下同)是最活泼的非金属元素;Ar是最不活泼的元素.
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的结构式H-O-H.
(4)比较⑤与⑥的化学性质,Na更活泼,试用实验证明(简述简单操作、主要现象和结论把钠镁分别投入冷水中,钠不断游动,不一会儿就消失,而镁无明显现象,故可知钠比镁活泼.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的结构式H-O-H.
(4)比较⑤与⑥的化学性质,Na更活泼,试用实验证明(简述简单操作、主要现象和结论把钠镁分别投入冷水中,钠不断游动,不一会儿就消失,而镁无明显现象,故可知钠比镁活泼.
10.聚氯乙烯简称PVC,是当今世界上产量最大、应用最广的热塑性塑料之一.下列说法正确的是( )
| A. | 聚氯乙烯的单体是CH3CH2Cl | |
| B. | 聚氯乙烯是高分子化合物 | |
| C. | 聚氯乙烯能够使溴的四氯化碳溶液褪色 | |
| D. | 聚氯乙烯保鲜膜最适合用来包装蔬菜、水果及熟食 |