题目内容
19.人体的胃酸是盐酸,胃酸过多的人常有胃痛、烧心的感觉.服用小苏打或胃舒平(主要成分为氢氧化铝)可解出胃痛,试写出服用上述两种药物所发生的离子反应方程式:HCO3-+H+=CO2↑+H2O,Al(OH)3+3H+=Al3++3H2O.如果病人同时伴有胃溃疡,此人最好服用胃舒平,理由是因产生CO2胃里压力增大而加剧胃壁穿孔.
分析 小苏打与盐酸反应生成氯化钠、水和二氧化碳;氢氧化铝与盐酸反应生成氯化铝和水.
解答 解:小苏打与盐酸反应生成氯化钠、水和二氧化碳,离子反应为HCO3-+H+=CO2↑+H2O,氢氧化铝与盐酸反应生成氯化铝和水,离子反应为Al(OH)3+3H+=Al3++3H2O,
故答案为:HCO3-+H+=CO2↑+H2O;Al(OH)3+3H+=Al3++3H2O;胃舒平;因服用小苏打产生CO2胃里压力增大而加剧胃壁穿孔.
点评 本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,注意化学与生活、药物的关系,题目难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
9.设NA代表阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA | |
| B. | Na2O2与H2O反应生成1.12L(标况)氧气,反应中转移电子的电子数为0.1NA | |
| C. | 1molNa与足量氧气反应,失去的电子数目为NA | |
| D. | 78gNa2O2固体中阴离子个数为2NA |
10.鲁米诺又名发光氨,广泛应用于刑事侦查、生物工程、化学示踪等领域.其制备方法之一如图: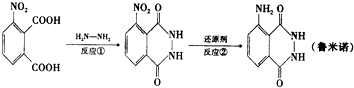
若反应②在催化剂作用下用H2还原,则制备1mol目标产物,理论上反应①与反应②生成水的质量比为( )

若反应②在催化剂作用下用H2还原,则制备1mol目标产物,理论上反应①与反应②生成水的质量比为( )
| A. | 1:2 | B. | 1:1 | C. | 2:1 | D. | 2:3 |
7.“84”消毒液有效成分为 NaClO,已知酸的电离平衡常数 H2CO3>HClO>HCO3- 下列说法正确的是( )
| A. | “84”消毒液可以与福尔马林溶液混合使用 | |
| B. | NaClO的稳定性和漂白性都比HClO强 | |
| C. | 工业上在特定条件下电解饱和食盐水制得NaClO,原理为:NaCl+H2O═NaClO+H2↑ | |
| D. | NaClO溶液在空气中发生离子反应为:2ClO-+CO2+H2O═2HClO+CO32- |
14.下列实验中,所选装置不合理的是( )
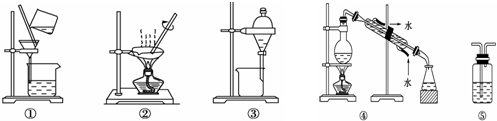

| A. | 分离Na2CO3溶液和苯,选④ | B. | 用CCl4提取碘水中的碘,选③ | ||
| C. | 用FeCl2溶液吸收Cl2,选⑤ | D. | 粗盐提纯,选①和② |
4.在下面的反应中,氨作为氧化剂参加反应的是( )
| A. | NH3+H3PO4═NH4H2PO4 | |
| B. | 4NH3+5O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$4NO+6H2O | |
| C. | 2NH3+3Cl2═6HCl+N2 | |
| D. | NH3+NaH═NaNH2+H2↑ |
11.下列反应的离子方程式书写正确的是( )
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 铝粉与氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ | |
| C. | 利用腐蚀法制作印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 在氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
8.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | S$→_{燃烧}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO4 | |
| B. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| C. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{通电}{→}$Mg | |
| D. | CuSO4(aq)$\stackrel{过量NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{葡萄糖}$Cu2O |
9.如图所示的A、B、C、D、E五种物质的相互关系,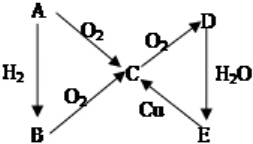 (有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
(有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
 (有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
(有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )| A. | N2 | B. | Cl2 | C. | S | D. | C |