题目内容
8.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )| A. | S$→_{燃烧}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO4 | |
| B. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| C. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{通电}{→}$Mg | |
| D. | CuSO4(aq)$\stackrel{过量NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{葡萄糖}$Cu2O |
分析 A、二氧化硫与氯化钡不反应;
B、二氧化硅不溶于水;
C、MgCl2•6H2O要在氯化氢的氛围中加热得到氯化镁固体;
D、硫酸铜和氢氧化钠反应生成氢氧化铜,氢氧化铜和葡萄糖加热反应生成氧化亚铜红色沉淀.
解答 解:A、二氧化硫与氯化钡不反应,弱酸不能制强酸,故A错误;
B、二氧化硅不溶于水,二氧化硅与水不反应,故B错误;
C、MgCl2•6H2O要在氯化氢的氛围中加热得到氯化镁固体,故C错误;
D、硫酸铜和氢氧化钠反应生成氢氧化铜,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,氢氧化铜和葡萄糖加热反应生成氧化亚铜红色沉淀,C6H12O6+2Cu(OH)2$\stackrel{加热}{→}$CH2(OH)(CHOH)4COOH+Cu2O↓+2H2O,所以能实现转化,故D正确;
故选D.
点评 本题考查了物质性质转化关系的分析判断,主要是我在性质和反应条件的分析应用,掌握元素化合物性质和反应实质是关键,题目难度中等.

练习册系列答案
相关题目
16.下列除去杂质的方法中正确的是( )
| A. | Cl2中混有少量HCl:通过盛有足量硝酸银溶液的洗气瓶洗气 | |
| B. | Cl2中混有少量水蒸气:先通过足量浓硫酸,再用向下排空气法收集氯气 | |
| C. | HCl中混有少量Cl2:通过盛有四氯化碳的洗气瓶洗气 | |
| D. | HCl中混有少量Cl2:通入足量氢气并光照 |
3.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
20.向100mL由等物质的量的FeBr2和FeI2配成的混合溶液中,缓慢通入氯气3.36L(标准状况),反应完全后,溶液中有一半的Fe2+被氧化成Fe3+,则原混合液中FeI2的物质的量浓度为( )
| A. | 0.5 moL•L-1 | B. | 1.0 moL•L-1 | C. | 1.2 moL•L-1 | D. | 1.5 moL•L-1 |
17.下表是25℃时四种酸的电离平衡常数:
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)25℃时,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5.
(3)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(4)25℃时,等物质的量浓度的HA、NaA混合溶液中,各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),.
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2,某同学分别取少量NaCl与NaNO2与试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法可行(填“可行”或“不可行”),理由是NaNO2+CH3COOH?CH3COONa+HNO2,2HNO2=H2O+NO+NO2,HNO2不稳定会分解,使平衡不断朝生成亚硝酸的方向移动,可观察到有红棕色气体产生,故此方法可行.
| 化学式 | CH3COOH | HA | HNO2 | H2CO3 |
| Ka | Ka=1.8×10-5 | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
(2)25℃时,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5.
(3)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(4)25℃时,等物质的量浓度的HA、NaA混合溶液中,各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),.
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2,某同学分别取少量NaCl与NaNO2与试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法可行(填“可行”或“不可行”),理由是NaNO2+CH3COOH?CH3COONa+HNO2,2HNO2=H2O+NO+NO2,HNO2不稳定会分解,使平衡不断朝生成亚硝酸的方向移动,可观察到有红棕色气体产生,故此方法可行.
20.下列图示的化学实验操作中,正确的是( )
| A. | 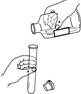 倾倒液体 | B. | 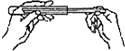 取粉末状固体药品 | ||
| C. | 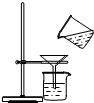 过滤 | D. | 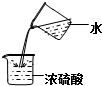 浓硫酸的稀释 |