题目内容
12.雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.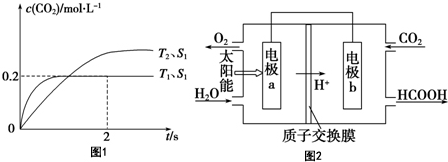
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示.
据此判断:
①该反应的△Η<0(填“>”或“<”),△S<0(填“>”或“<”)
②在T1温度下,0~2s内的平均反应速率v(N2)=0.05mol/(L•s).
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若增大催化剂的表面积,则CO转化率不变(填“增大”,“减少”或“不变”)
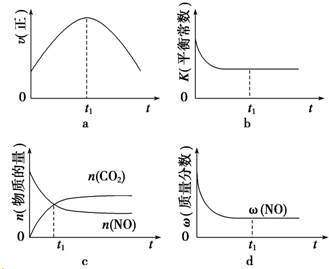
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd(填字母).
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
例如:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867.0kJ•mol-1
2NO2(g)?N2O4(g)△H=-56.9kJ•mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(g)的热化学方程式CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),△H=-810.1kJ/mol.
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.图2是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图.电极a、b表面发生的电极反应式分别为
a:2H2O-4e-═O2↑+4H+,
b:2CO2+4H++4e-=2HCOOH.
分析 (1)①根据到达平衡的时间判断温度高低,根据平衡时二氧化碳的浓度判断温度对平衡的影响,进而判断△H;
②由图可知,T2温度平衡时,二氧化碳的浓度变化量为0.1mol/L,根据v=$\frac{△c}{△t}$计算v(CO2),再根据速率之比等于化学计量数之比计算v(N2);
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动;
④a、到达平衡后正、逆速率相等,不再变化;
b、到达平衡后,温度为定值,平衡常数不变,结合反应热判断随反应进行容器内温度变化,判断温度对化学平衡常数的影响;
c、t1时刻后二氧化碳、NO的物质的量发生变化,最后不再变化;
d、到达平衡后各组分的含量不发生变化;
(2)①根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式;
②由图可知,左室投入水,生成氧气与氢离子,电极a表面发生氧化反应,为负极,右室通入二氧化碳,酸性条件下生成HCOOH,电极b表面发生还原反应,为正极.
解答 解:(1)①由图1可知,温度T1先到达平衡,故温度T1>T2,温度越高平衡时,二氧化碳的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0,2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g),反应前后气体体积减小,反应熵变△S<0,
故答案为:<;<;
②由图可知,T2温度时2s到达平衡,平衡时二氧化碳的浓度变化量为0.2mol/L,故v(CO2)=$\frac{0.2mol/L}{2s}$=0.1mol/(L•s),速率之比等于化学计量数之比,故v(N2)=$\frac{1}{2}$v(CO2)=$\frac{1}{2}$×0.1mol/(L•s)=0.05mol/(L•s),
故答案为:0.05mol/(L•s);
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,一氧化碳的转化率不变,故答案为:不变;
④a、到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故a错误;
b、该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图象与实际符合,故b正确,
c、t1时刻后二氧化碳、NO的物质的量发生变化,t1时刻未到达平衡状态,故c错误;
d、NO的质量分数为定值,t1时刻处于平衡状态,故d正确;
故答案为:bd;
(2)①已知:Ⅰ、CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol
Ⅱ、2NO2(g)?N2O4(g)△H2=-56.9kJ/mol
根据盖斯定律,Ⅰ-Ⅱ得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)=-810.1kJ/mol,
即CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),△H=-810.1kJ/mol;
②由图可知,左室投入水,生成氧气与氢离子,电极a表面发生氧化反应,为负极,电极反应式为2H2O-4e-═O2↑+4H+,右室通入二氧化碳,酸性条件下生成HCOOH,电极b表面发生还原反应,为正极,电极反应式为2CO2+4e-+4H+═2HCOOH,
故答案为:2H2O-4e-═O2↑+4H+;2CO2+4H++4e-=2HCOOH.
点评 本题考查化学平衡图象、化学反应速率、影响化学平衡的因素、热化学方程式书写、原电池、电离平衡常数与水解平衡常数等,题目综合性较大,难度中等,是对知识的综合利用、注意基础知识的理解掌握.

 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案| A. | 氯碱工业制烧碱:2Cl-+2H2O═H2↑+Cl2↑+2OH- | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+OH-$→_{△}^{H_{2}O}$CH2=CH2↑+Br-+H2O | |
| C. | 向苯酚溶液中滴加过量浓溴水: | |
| D. | 乙醛和含NaOH的新制Cu(OH)2悬浊液共热:2Cu(OH)2+CH3CHO+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+3H2O |
| A. | 加金属钠看是否有氢气放出 | |
| B. | 与新制的氢氧化铜悬浊液混合后共热,观察是否有红色沉淀 | |
| C. | 与醋酸和浓H2SO4共热,观察是否有果香味物质生成 | |
| D. | 加入酸性KMnO4溶液,看溶液是否褪色 |
 某学生对Na2SO3与AgNO3在不同pH下的反应进行探究.
某学生对Na2SO3与AgNO3在不同pH下的反应进行探究.(1)测得Na2SO3溶液pH=10,AgNO3溶液pH=5,二者发生水解的离子分别是SO32-、Ag+.
(2)调节pH,实验记录如下:
| 实验 | pH | 现象 |
| A | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
| B | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
| C | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
①Ag2SO3:白色,难溶于水,溶于过量Na2SO3的溶液
②Ag2O:棕黑色,不溶于水,能和酸反应,它和盐酸反应的化学方程式为:Ag2O+2HCl=2AgCl+H2O.
(3)该同学推测a中白色沉淀为Ag2SO4,依据是空气中的氧气可能参与反应,则生成硫酸银沉淀的离子方程式为2Ag++O2+2SO32-=Ag2SO4↓+SO42-.
该同学设计实验确认了A、B、C中的白色沉淀不是Ag2SO4,实验方法是:取B、C中白色沉淀,置于Na2SO3溶液中,沉淀溶解.另取Ag2SO4固体置于足量Na2SO3溶液中,未溶解.
(4)将C中X滤出、洗净,为确认其组成,实验如下:
I.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓HNO3,产生红棕色气体
Ⅲ.用Ba(NO3)2溶液、BaCl2溶液检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验I的目的是证明X不是Ag2O.
②根据实验现象,分析X是Ag.
③Ⅱ中反应的化学方程式是Ag+2HNO3(浓)=AgNO3+NO2↑+H2O.
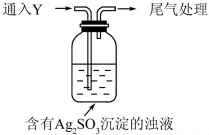
(5)该同学综合以上实验,分析产生X的原因,认为随着酸性的增强.+4价硫的还原性增强,能被+1价银氧化.通过进一步实验确认了这种可能性,实验如下:
①通入Y后,瓶中白色沉淀转化为棕黑色,气体Y是SO2.
②白色沉淀转化为X的化学方程式是Ag2SO3+H2O$\stackrel{H+}{→}$2Ag+H2SO4.
| A. | 称取碳酸钠晶体53.0g | |
| B. | 移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 | |
| C. | 定容时,俯视观察刻度线 | |
| D. | 定容后,将容量瓶反复倒转、摇匀、静置时发现液面低于刻度线,于是又加入少量水至刻度线 |
 “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
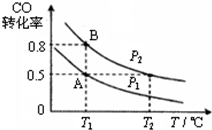
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.(1)向体积为 2L的密闭容器中充入1mol CO和2mol H2,在一定条件下发生如下反应:CO(g)+2H2(g)?CH3OH(g).经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如图所示.请回答:
①p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为$\frac{0.5}{t}$mol•L-1•s-1
②图中压强p1< 压强p2.(填“>”、“<”或“=”)
(2)一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
| 容器 编号 | 温度(℃) | 起始的物质的量(mol) | 平衡的物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②达到平衡时,容器I中的CH3OH的体积分数相等(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数.
③若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行(填“正反应”、“逆反应”或“不移动”).
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).若反应在恒容绝热(不
与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高.
| 物质 | CO2 | H2 | CH3OH | H2O |
| 起始投料/mol | 1 | 3 | 2 | 0 |

