题目内容
12.下列反应中能用于检验尿液中是否含有葡萄糖的是( )| A. | 加金属钠看是否有氢气放出 | |
| B. | 与新制的氢氧化铜悬浊液混合后共热,观察是否有红色沉淀 | |
| C. | 与醋酸和浓H2SO4共热,观察是否有果香味物质生成 | |
| D. | 加入酸性KMnO4溶液,看溶液是否褪色 |
分析 A.尿液中含水,无论是否含葡萄糖,加入钠都会有氢气放出;
B.葡萄糖中含有醛基,能够与新制的氢氧化铜浊液反应生成红色的氧化亚铜沉淀;
C.尿液中葡萄糖含量很低,与醋酸反应不明显;
D.尿液中含有尿素等具有还原性物质,也能够使酸性高锰酸钾溶液褪色.
解答 解:A.钠化学性质比较活泼,能够与水发生反应,所以无法用钠鉴别尿液中是否含有葡萄糖,故A错误;
B.葡萄糖和氢氧化铜在碱性溶液中加热会生成砖红色的氧化亚铜,所以加入新制的氢氧化铜悬浊液加热,观察是否有砖红色的沉淀生成,可以检验糖尿病病人的尿液中是否含有葡萄糖,故B正确;
C.尿液中葡萄糖含量很低,与醋酸反应不明显;且尿液具有刺激性气味,也无法判断是否有果香味物质生成,故C错误;
D.尿液中含有的其它还原性物质能够使酸性高锰酸钾溶液褪色,无法用酸性KMnO4溶液鉴别,故D错误;
故选B.
点评 本题考查了据此有机物的鉴别方法,题目难度中等,明确葡萄糖的结构与性质为解答关键,注意掌握常见有机物性质及鉴别方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
2.已知反应H2(g)+Br2(g)=2HBr(g)△H=-83kJ•mol-1,1molH2(g)、1molBr2(g) 分子中化学键断裂时分别需要吸收436kJ、193kJ的能量,则断开1molHBr(g) 分子中化学键需吸收的能量为( )
| A. | 566kJ | B. | 283kJ | C. | 712kJ | D. | 356kJ |
3.“宽带中国”战略的阶段性发展目标指出,2015年要基本实现城市光纤到楼入户、农村宽带进乡入村,光纤到户(FTTH)要达0.7亿用户.光纤(光导纤维的简称)的主要成分是( )
| A. | 晶体硅 | B. | 二氧化硅 | C. | 硅酸钠 | D. | 铝硅合金 |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L D2中所含中子数为2NA | |
| B. | 1 molCO2与1L 2mol/L的NaOH溶液反应后,溶液中的CO32-数为0.5 NA | |
| C. | 6.8g熔融的KHSO4中含有0.1NA个阳离子 | |
| D. | 3.36L氯气与2.7g铝充分反应,转移电子数一定为0.3NA |
5.化学与生活密切相关,下列说法不正确的是( )
| A. | 煤、石油、天然气是不可再生能源,风能、生物质能、沼气是可再生能源 | |
| B. | “84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感 | |
| C. | 已知水热反应是指在高温高压下,将二氧化碳转化为有机物的技术,则水热反应可以降低自然界中碳的含量 | |
| D. | 已知PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,则PM2.5在空气中有可能形成胶体 |
9.下列说法不正确的是( )
| A. | 淀粉、纤维素水解的最终产物都是葡萄糖 | |
| B. | 误服可溶性重金属盐,立即服用大量牛奶可以解毒 | |
| C. | 用灼烧的方法可鉴别毛织物和棉织物 | |
| D. | 温度越高,酶对某些化学反应的催化效率越高 |
10.一定条件下,在密闭容器里进行如下可逆反应:S2Cl2(橙黄色液体)+Cl2(气)?2SCl2(鲜红色液体)△H=-61.16kJ•mol-1.下列说法正确的是( )
| A. | 增大压强,平衡常数将增大 | |
| B. | 达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 | |
| C. | 达到平衡时,若升高温度,氯气的百分含量减小 | |
| D. | 加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
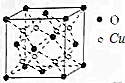 科学家研究发现金属离子吸收氧气的能力十分巨大,人体血液中的血红蛋白依靠亚铁离子结合氧气,其他金属离子(Cu2+、Zn2+等)也可以实现结合和运输氧气的目的.最近丹麦科学家研发了一种晶体材料,该晶体吸收氧气的能力依靠钴离子,它可以让人在水下持久地获得氧气.
科学家研究发现金属离子吸收氧气的能力十分巨大,人体血液中的血红蛋白依靠亚铁离子结合氧气,其他金属离子(Cu2+、Zn2+等)也可以实现结合和运输氧气的目的.最近丹麦科学家研发了一种晶体材料,该晶体吸收氧气的能力依靠钴离子,它可以让人在水下持久地获得氧气.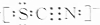 ,则SCN-中σ 键与π键的个数比为1:1.
,则SCN-中σ 键与π键的个数比为1:1.