题目内容
18.关于亚硝酸钠与氯化钠,下列叙述正确的是( )| A. | 因亚硝酸钠有剧毒,所以不能用作食品添加剂 | |
| B. | 可用淀粉-KI试纸来鉴别一种盐溶液是亚硝酸钠还是氯化钠 | |
| C. | 能用硝酸银溶液来区别亚硝酸钠与氯化钠 | |
| D. | 因NaNO2具有较强的氧化性,可用酸性KMnO4溶液和FeCl2溶液鉴别NaCl与NaNO2 |
分析 A.亚硝酸盐可做防腐剂和肉类制品的发色剂,因有毒量要严加控制;
B、NaNO2具有氧化性,在酸性条件下氧化碘化钾,得到单质碘,单质碘遇淀粉溶液变蓝,而NaCl无氧化性;
C、亚硝酸银和氯化银均为白色沉淀;
D、酸性高锰酸钾具有极强的氧化性,能氧化NaNO2.
解答 解:A.防腐剂是用以保持食品原有品质和营养价值为目的食品添加剂,它能抑制微生物活动、防止食品腐败变质从而延长保质期,食品防腐剂亚硝酸钠有毒,长期食用会对身体有害,所以不得超标准使用,故A错误;
B、NaNO2具有氧化性,在酸性条件下氧化碘化钾,得到单质碘,单质碘遇淀粉溶液变蓝,NaCl无氧化性,在酸性条件下不能氧化碘化钾,所以可用淀粉碘化钾试纸和食醋鉴别NaCl与NaNO2,故B正确;
C、亚硝酸银和氯化银均为白色沉淀,所以不能用硝酸银溶液来区别亚硝酸钠与氯化钠,故C错误;
D、酸性高锰酸钾具有极强的氧化性,能氧化NaNO2,所以不能用酸性高锰酸钾鉴别NaCl与NaNO2,两者都能使酸性高锰酸钾褪色,故D错误;
故选B.
点评 本题主要考查了亚硝酸盐的性质、高锰酸钾的性质等知识,掌握亚硝酸的性质是解答的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列反应中,属于氧化还原反应的是( )
| A. | 氢氧化铝受热分解 | |
| B. | 氧化铜与硝酸反应 | |
| C. | 实验室中用高锰酸钾加热分解制取 氧气 | |
| D. | 实验室中用氯化铵固体与氢氧化钙固体制取氨气 |
6.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 常温常压下,14.2克 Na2SO4含有的Na+离子数为0.2NA | |
| B. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| C. | 通常状况下,NA个N2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为NA |
13.实验中的下列操作正确的是( )
| A. | 从试剂瓶中取出的一些Na2CO3溶液放入试管中,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 稀释浓硫酸时,应将浓硫酸倒入水中,边加边搅拌 | |
| C. | 用蒸发方法使NaCl从溶液里析出,应将蒸发皿中NaCl溶液全部蒸干才停止加热 | |
| D. | 分液操作中,分液漏斗中下层液体从下口放出,上层液体也从下口倒出 |
3.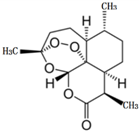 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素属于芳香化合物,能与H2发生加成反应 | |
| B. | 青蒿素能与氢氧化钠溶液发生反应 | |
| C. | 青蒿素的化学式为C15H22O5 | |
| D. | 青蒿素的核磁共振谱图中有12个峰 |
10. X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
 X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )| A. | 洗气瓶中产生的沉淀是亚硫酸钡 | B. | 洗气瓶中产生的沉淀是碳酸钡 | ||
| C. | 洗气瓶中没有明显现象 | D. | 洗气瓶中有硫酸钡沉淀 |
1.对于反应A(g)+3B(g)?2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
| A. | v(A)═0.01 mol/(L•s) | B. | v (B)═0.02 mol/(L•s) | ||
| C. | v (B)═0.60mol/(L•min) | D. | v (C)═1.0mol/(L•min) |