题目内容
12.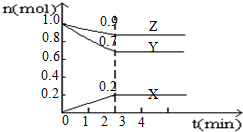 某温度时,在4L的容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在4L的容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.(1)由图中数据分析,该反应的化学方程式为:3Y+Z?2X
(2)反应从开始至2min内X的平均反应速率是:0.025mol/(L•min)
(3)反应过程中Y的转化率:30%
(4)2min后图象所表示的含义该反应在该条件下,已达到化学平衡状态.
分析 (1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
(2)根据v=$\frac{△c}{△t}$,计算反应速率;
(3)根据转化率=$\frac{转化量}{起始量}$×100%来计算求解;
(4)根据平衡时各组分的物质的量不变这一特征作判断.
解答 解:(1)由图象可以看出,反应中Y、Z的物质的量减小,X的物质的量增多,则Y、Z为反应物,X为生成物,且△n(Z):△n(Y):△n(X)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为3Y+Z?2X,
故答案为:3Y+Z?2X;
(2)v(X)=$\frac{\frac{0.2mol}{4L}}{2min}$=0.025mol•(L•min)-1,故答案为:0.025mol/(L•min);
(3)根据转化率=$\frac{转化量}{起始量}$×100%=$\frac{1-0.7}{1}$×100%=30%,故答案为:30%;
(4)根据图象可知,当在2mim时,反应中各组份的物质的量不再随时间变化而变化,此时反应达到平衡状态,故答案为:该反应在该条件下,已达到化学平衡状态.
点评 本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法及基本公式的应用.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
4.英国路透社曾报道:以色列军方已经研制出一种新的刺激性非致命武器,可用来驱散抗议者,这种新武器叫臭鼬弹.已知臭鼬剂主要成分是丁硫醇(C4H9SH),人的口臭是由于分泌出有臭味的甲硫醇(CH3SH),液化气中添加的报警剂是极臭的乙硫醇(C2H5SH).下列说法你认为不正确的是( )
| A. | 丁硫醇、甲硫醇与乙硫醇互为同系物 | |
| B. | 沸点不同的丁硫醇有四种 | |
| C. | 丁硫醇在空气中燃烧生成二氧化碳、二氧化硫和水 | |
| D. | 在水溶液中,乙硫醇比乙醇更难电离出H+离子 |
1.下列叙述正确的是( )
| A. | 钠的金属活泼性大于铜,在溶液中钠可以置换出铜 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入KNO3固体,铜粉仍不溶解 | |
| C. | 在KI溶液中加入NaNO3,没有明显现象,加入盐酸,即有I2生成 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较,加入少量CuSO4固体,速率不改变 |
2.将铜丝放在酒精灯上加热片刻后,立即浸入乙醇中,反复多次可观察到的现象是( )
| A. | 铜丝在乙醇中变黑 | B. | 铜丝点燃后变红 | ||
| C. | 反应中产生黑烟 | D. | 铜丝在乙醇中变红 |
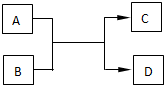 学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.
学习了元素周期表,可以帮助我们进一步丰富不同元素间的相互转化关系.已知A、B、C、D都处于短周期,A、D为单质,B、C是化合物.