题目内容
3.下列各组物质的晶体中,化学键和晶体类型完全相同的是( )| A. | 二氧化碳和二氧化硅 | B. | 氯化钠和氯化氢 | ||
| C. | 氢氧化钾和氯化钾 | D. | 二氧化硫和水 |
分析 根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键,金属单质含有金属键.
解答 解:A.固体二氧化碳是分子晶体,二氧化硅是原子晶体,二氧化硅、二氧化碳都只含共价键,故A错误;
B.氯化钠为离子晶体,含有离子键,氯化氢为分子晶体,含有共价键,故B错误;
C.氢氧化钾含有离子键和共价键,氯化钾含有离子键,故C错误;
D.二氧化硫和水都为共价化合物,含有共价键,且晶体类型为分子晶体,故D正确.
故选D.
点评 本题考查了化学键类型和晶体类型的关系,注意判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键,题目难度不大.

练习册系列答案
相关题目
14.下列变化或应用中,与分子间作用力有关的是( )
| A. | 臭氧转变为氧气 | |
| B. | 工业生产中氯化钠晶体的熔化、冷却 | |
| C. | 夏天马路洒水降温 | |
| D. | 日本大地震中用次氯酸溶液进行环境消毒 |
11.盛有氯化钡稀溶液的甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量氯水,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是( )
| A. | 甲、乙两试管都有白色沉淀生成 | B. | 甲、乙两管都没有白色沉淀生成 | ||
| C. | 甲管没有白色沉淀生成而乙试管有 | D. | 甲管有白色沉淀而乙试管没有 |
18.把aL含硫酸铵和硝酸铵的混合溶液分成两等份,一份需用bmol烧碱刚好把氨气全部赶出,另一份与氯化钡反应时,消耗BaCl2cmol,则原溶液中NO3-的物质的量浓度是( )
| A. | $\frac{(b-2c)}{a}$mol/L | B. | $\frac{(2b-c)}{a}$ mol/L | C. | $\frac{(2b-2c)}{a}$ mol/L | D. | $\frac{(2b-4c)}{a}$ mol/L |
15.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4 L任意比的O2和N2的混合气体中含有的分子总数均为NA | |
| B. | 标准状况下,14 g氮气含有的氮原子数为0.5NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 标准状况下,22.4LH2O所含有的电子数是10NA |
12.目前,科学界拟合成一种“双重结构”的球形分子,即把足球烯C60的分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列叙述错误的是( )
| A. | 该晶体为原子晶体 | B. | 该物质的熔沸点较低 | ||
| C. | 该物质是新化合物 | D. | 该物质的相对分子量质量为2400 |
 日常生活中,我们经常饮用矿泉水.如图是某饮用天然水部分商标图,图中列出了理化指标.我据此回答:这里的钙、镁、钾、钠指的是( )
日常生活中,我们经常饮用矿泉水.如图是某饮用天然水部分商标图,图中列出了理化指标.我据此回答:这里的钙、镁、钾、钠指的是( )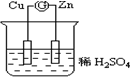 如图所示的原电池装置中,锌为负极,电极发生的是氧化反应(填氧化或还原),电极反应式为Zn-2e-=Zn2+;铜电极反应式为2H++2e-=H2↑,铜片上观察到的现象为有气泡产生.
如图所示的原电池装置中,锌为负极,电极发生的是氧化反应(填氧化或还原),电极反应式为Zn-2e-=Zn2+;铜电极反应式为2H++2e-=H2↑,铜片上观察到的现象为有气泡产生.