题目内容
2.下列与有机物结构、性质相关的叙述错误的是( )| A. | 乙酸分子中含有羧基,可与Na2CO3溶液反应生成CO2 | |
| B. | 淀粉和纤维素都属于高分子化合物 | |
| C. | 苯不能使酸性高锰酸钾褪色 | |
| D. | 苯分子中不存在碳碳双键所以不能发生加成反应 |
分析 A.乙酸含有羧基,酸性比碳酸强;
B.淀粉和纤维素属于多糖,相对分子质量大于10000;
C.苯性质稳定,与高锰酸钾不反应;
D.苯可发生加成反应.
解答 解:A.乙酸含有羧基,酸性比碳酸强,可与碳酸钠反应,故A正确;
B.淀粉和纤维素属于多糖,相对分子质量大于10000,属于高分子化合物,故B正确;
C.苯性质稳定,与高锰酸钾不反应,故C正确;
D.苯不含碳碳双键,但可发生加成反应,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,题目难度不大,注意把握有机物的结构和性质,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
13.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入稀盐酸溶液没有产生白色沉淀,再加入氯化钡溶液有白色沉淀产生,一定有SO42- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
10.如图装置可用来收集下列某种气体,该气体是( )
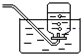

| A. | SO2 | B. | Cl2 | C. | O2 | D. | HCl |
14. 过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
(1)实验室利用反应2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑可制备氧气.
①取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如表所示.
实验1、2研究的是温度对H2O2分解速率的影响.
实验2、3的目的是比较FeCl3溶液和MnO2作为催化剂对H2O2分解反应速率影响的差异.
实验中可以表明该反应速率差异的现象是产生气泡的快慢.
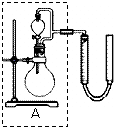
②实验室用MnO2做该反应的催化剂,使用如图所示装置的A部分制备O2,避免反 应过于剧烈的操作是旋转分液漏斗的活塞,控制滴加H2O2溶液的速率.
(2)Na2O2与水反应也可生成O2.某同学取4g Na2O2样品与过量水反应,待反应完全终止时,得100mL溶液X和448mL O2(已折算为标准状况).该同学推测样品中含有杂质或反应中生成H2O2,并进行实验研究.
①取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀.则反应的离子方程式是2Fe2++4OH-+H2O2=2Fe(OH)3↓.
②通过如图所示整套实验装置测定Na2O2样品的纯度,假设所含杂质不参加反应.取25mL X,滴入烧瓶内使其与过量KMnO4酸性溶液反应,最终生成56mL O2(已折算为标准状况),则此样品中Na2O2的质量分数是97.5%.
 过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.(1)实验室利用反应2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑可制备氧气.
①取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如表所示.
| 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | |||
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 | ||
实验2、3的目的是比较FeCl3溶液和MnO2作为催化剂对H2O2分解反应速率影响的差异.
实验中可以表明该反应速率差异的现象是产生气泡的快慢.
②实验室用MnO2做该反应的催化剂,使用如图所示装置的A部分制备O2,避免反 应过于剧烈的操作是旋转分液漏斗的活塞,控制滴加H2O2溶液的速率.
(2)Na2O2与水反应也可生成O2.某同学取4g Na2O2样品与过量水反应,待反应完全终止时,得100mL溶液X和448mL O2(已折算为标准状况).该同学推测样品中含有杂质或反应中生成H2O2,并进行实验研究.
①取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀.则反应的离子方程式是2Fe2++4OH-+H2O2=2Fe(OH)3↓.
②通过如图所示整套实验装置测定Na2O2样品的纯度,假设所含杂质不参加反应.取25mL X,滴入烧瓶内使其与过量KMnO4酸性溶液反应,最终生成56mL O2(已折算为标准状况),则此样品中Na2O2的质量分数是97.5%.
12.我国铁路将进入高铁时代.为适应提速要求需把短轨连成长轨,常用反应:xAl+Fe2O3 $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+xFe进行焊接,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.下列说法不正确的是( )
| A. | Al2O3为氧化物 | B. | 该反应为置换反应 | ||
| C. | 该反应方程式中的x为3 | D. | 该反应会放出大量热 |
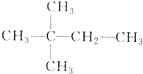 ,则A的结构简式为
,则A的结构简式为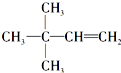 ;A加氢产物的一氯代物有3种.
;A加氢产物的一氯代物有3种.