题目内容
16.在一定温度下,将3mol CO和6mol H2O(g)充入一密闭容器中发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应达到平衡后,测得CO2的物质的量为2mol.然后再充入9mol H2O(g),达到新的平衡后,体系中CO、H2O(g)、CO2、H2总的物质的量为( )| A. | 15.5 mol | B. | 18 mol | C. | 20.5 mol | D. | 无法计算 |
分析 反应CO+H2O(g)?CO2+H2达平衡后,加入水蒸气,化学平衡会向着正反应方向进行,但是反应物不可能全部转化为生成物.
解答 解:根据题意:CO+H2O(g)??CO2 +H2,
初始物质的量:3 6 0 0
变化物质的量:2 2 2 2
平衡物质的量:1 4 2 2
此时二氧化碳和氢气的物质的量之和是4mol,再通入9mol水蒸气,化学平衡会向着正反应方向进行,假设一氧化碳全部转化完毕,则会生成二氧化碳和氢气各1mol,此时新生成的CO2和H2的物质的量之和是2mol,剩余水蒸气12mol,但是一氧化碳不会全部转化,所以达到新的平衡后,体系中CO、H2O(g)、CO2、H2总的物质的量小于18mol,
故选A.
点评 本题考查学生可逆反应的特征以及化学平衡移动方面的知识,注意知识的积累是解题的关键,难度不大.

练习册系列答案
相关题目
6.下列说法一定正确的是( )
| A. | 酸性物质与酸性物质、碱性物质与碱性物质不能反应 | |
| B. | 溶液中某离子浓度减小发生了化学反应 | |
| C. | 含同一元素的不同化合物,该元素的化合价越高,其氧化性越强 | |
| D. | 多个电解池串联,通过每个电极电子的物质的量相等 |
7.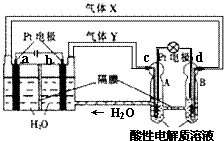 “天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
“天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
 “天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
“天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | 当转移0.1 mol电子,a极产生2.24 L H2 | |
| B. | b电极反应是:4H2O+4e-═2H2↑+4OH- | |
| C. | d电极反应是:O2+4H++4e-═2H2O | |
| D. | c极上发生还原反应,B中H+经隔膜进入A |
1.分别中和10mL1.0mol/L的HCl溶液,消耗了等体积的氢氧化钠溶液和氨水溶液,则氢氧化钠溶液和氨水溶液的关系是( )
| A. | 所含溶质质量相等 | B. | 所含溶质物质的量氨水多 | ||
| C. | 溶液物质的量浓度相等 | D. | 电离度相等 |
8.环境污染已成为人类社会面临的重大威胁,各种污染数不胜数,下列各项中与环境污染无关的是( )
| A. | 温室效应 | B. | 水华 | C. | 臭氧空洞 | D. | 潮汐 |
5.鉴别下列各组物质所用的试剂或方法不正确的是( )
| A. | 硬水、软水(肥皂水) | B. | 稀盐酸、食盐水(酚酞试液) | ||
| C. | 涤纶、羊毛制品(点燃) | D. | 空气、氧气(带火星的木条) |
6.人体正常的血红蛋白应含Fe2+.若误食外表与食盐相近的亚硝酸盐,则导致血红蛋白中的Fe2+转化成Fe3+而中毒,服用维生素C可解除亚硝酸盐中毒,下列叙述中正确的是( )
| A. | 亚硝酸盐是还原剂 | B. | 维生素C是还原剂 | ||
| C. | 维生素C是氧化剂 | D. | 亚硝酸盐被氧化 |