题目内容
称取两份铝粉,第一份加入足量的浓NaOH(aq),第二份加入足量的HCl(aq),如果放出等体积的气体(在同温同压下),则两份铝粉的质量之比为( )
| A、2:3 | B、1:1 |
| C、1:2 | D、1:3 |
考点:铝的化学性质,化学方程式的有关计算
专题:计算题
分析:铝与盐酸反应的化学方程式为:2Al+6HCl=2AlCl3+3H2↑,铝与NaOH溶液反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,假设生成的氢气的物质的量为3mol,结合方程式计算.
解答:
解:设生成的氢气的物质的量为3mol,
则:2Al+6HCl=2AlCl3+3H2↑,
2 3
2mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2 3
2nmol 3mol
则消耗两份铝粉的质量之比为 2mol:2mol=1:1,
故选B.
则:2Al+6HCl=2AlCl3+3H2↑,
2 3
2mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2 3
2nmol 3mol
则消耗两份铝粉的质量之比为 2mol:2mol=1:1,
故选B.
点评:本题考查了铝的化学性质、化学方程式的简单计算,题目难度不大,注意掌握常见化学关方程式的书写,能够根据化学方程式解决简单的化学计算.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
原计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir〕元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素是
Ir,则其核内的质量数是( )
191 77 |
| A、77 | B、286 |
| C、191 | D、114 |
某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
| A、21:5 | B、11:3 |
| C、3:1 | D、4:1 |
下列反应中,最终一定有白色沉淀生成的是( )
①向Na2SO4溶液中加入稀盐酸酸化后,再加入BaCl2溶液;
②向Na2SiO3溶液中通入过量的CO2;
③向Ca(OH)2溶液中通入过量的CO2;
④向BaCl2溶液中通入少量的SO2;
⑤向Ba(NO3)2溶液中通入过量的SO2.
①向Na2SO4溶液中加入稀盐酸酸化后,再加入BaCl2溶液;
②向Na2SiO3溶液中通入过量的CO2;
③向Ca(OH)2溶液中通入过量的CO2;
④向BaCl2溶液中通入少量的SO2;
⑤向Ba(NO3)2溶液中通入过量的SO2.
| A、①② | B、①③④ |
| C、①②⑤ | D、②③④ |
正确量取7.5mL液体,应选用的一组仪器是( )
①5mL量筒②10mL量筒③20mL量筒④胶头滴管.
①5mL量筒②10mL量筒③20mL量筒④胶头滴管.
| A、③④ | B、①②④ |
| C、②④ | D、只有③ |
下列有机物的命名正确的是( )
A、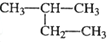 2-乙基丙烷 2-乙基丙烷 |
| B、CH3-CH=CH-CH3 2-丁烯 |
C、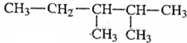 3,4─二甲基戊烷 3,4─二甲基戊烷 |
D、 二甲基苯 二甲基苯 |
盐类的水解过程中正确的说法是( )
| A、盐的电离平衡破坏 |
| B、水的电离平衡发生移动 |
| C、溶液的PH减小 |
| D、没有发生中和反应 |
A、B属于短周期中不同主族的元素,A、B原子的最外层电子中,成对电子和未成对电子占据的轨道数相等,若A元素的原子序数为a,则B元素的原子序数不可能为( )
| A、a-4 | B、a-5 |
| C、a+3 | D、a+11 |