题目内容
某化学研究性学习小组在实验室中模拟海水提取溴的过程如下:
海水
Br2(g)
[NaBr NaBrO3]
Br2
(1)取24L除去悬浮杂质后的海水,浓缩至2L.浓缩的目的是 .
(2)向浓缩后的溶液中通入足量Cl2,反应的离子方程式为 ,通入热空气的目的是 .
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,反应的化学方程式为 ,将产生的CO2全部通入足量澄清石灰水中,得到1g白色沉淀.
(4)假设整个过程中没有溴元素的损失,则该海水中溴的浓度为 g?L-1.
海水
| 除去悬浮 |
| 杂质 |
| 浓缩 |
| 氧化剂 |
| 氧化 |
| 热空气 |
| Na2CO3溶液 |
| 吸收 |
| H2SO4 |
(1)取24L除去悬浮杂质后的海水,浓缩至2L.浓缩的目的是
(2)向浓缩后的溶液中通入足量Cl2,反应的离子方程式为
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,反应的化学方程式为
(4)假设整个过程中没有溴元素的损失,则该海水中溴的浓度为
考点:海水资源及其综合利用
专题:化学应用
分析:(1)海水淡化得到母液和电解氯化钠溶液可生成氯气,得到的溴单质浓度低,溴单质在水中有一定的溶解性且和水反应,提取时消耗过的能源和原料,降低了经济效益;
(2)根据氯气具有氧化性,能氧化溴离子生成单质溴;根据溴易挥发;
(3)根据反应物、生成物,利用化合价升降总数相等和质量守恒来配平;
(4)根据Br-和BrO3-在酸性条件下发生归中反应生成Br2;根据各步反应,可确定如下关系:CaCO3~CO2~Br2,根据CaCO3的质量求出Br2的质量,根据C=
来计算.
(2)根据氯气具有氧化性,能氧化溴离子生成单质溴;根据溴易挥发;
(3)根据反应物、生成物,利用化合价升降总数相等和质量守恒来配平;
(4)根据Br-和BrO3-在酸性条件下发生归中反应生成Br2;根据各步反应,可确定如下关系:CaCO3~CO2~Br2,根据CaCO3的质量求出Br2的质量,根据C=
| m |
| V |
解答:
解:(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,
故答案为:富集溴元素;
(2)因氯气具有氧化性,能氧化溴离子生成单质溴:Cl2+2Br-═Br2+2Cl-;
因溴易挥发,所以一般用热空气或水蒸气将Br2吹出,
故答案为:Cl2+2Br-═Br2+2Cl-;将Br2吹出;
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,生成一个NaBr化合价降低1,生成一个NaBrO3化合价升高5,根据化合价升降总数相等和质量守恒来配平得:3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑,
故答案为:3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑;
(4)将产生的CO2全部通入足量澄清石灰水中,得到1g白色沉淀,通过反应Cl2+2Br-═Br2+2Cl-置换出溴单质后,一般用热空气或水蒸气将Br2吹出;根据各步反应,可确定如下关系:Br2~CO2~CaCO3,根据CaCO3的质量
可求出原24L海水中Br2的质量为
=1.6 g,
则海水中溴的浓度为
=0.067 g/L,
故答案为:0.067.
故答案为:富集溴元素;
(2)因氯气具有氧化性,能氧化溴离子生成单质溴:Cl2+2Br-═Br2+2Cl-;
因溴易挥发,所以一般用热空气或水蒸气将Br2吹出,
故答案为:Cl2+2Br-═Br2+2Cl-;将Br2吹出;
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,生成一个NaBr化合价降低1,生成一个NaBrO3化合价升高5,根据化合价升降总数相等和质量守恒来配平得:3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑,
故答案为:3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑;
(4)将产生的CO2全部通入足量澄清石灰水中,得到1g白色沉淀,通过反应Cl2+2Br-═Br2+2Cl-置换出溴单质后,一般用热空气或水蒸气将Br2吹出;根据各步反应,可确定如下关系:Br2~CO2~CaCO3,根据CaCO3的质量
可求出原24L海水中Br2的质量为
| 160g/mol×1g |
| 100g/mol |
则海水中溴的浓度为
| 1.6g |
| 24L |
故答案为:0.067.
点评:本题结合海水提取溴的过程,考查了氧化还原反应、化学计算、方程式的书写,难度中等,在配平时抓住化合价升降总数相等.

练习册系列答案
相关题目
已知X、Y分别为同周期的ⅠA和 VIA族的两种元素,它们的原子序数分别为a和b,则下列关系不可能成立的是( )
| A、a=b-15 |
| B、a=b-29 |
| C、a=b-9 |
| D、a=b-5 |
下列有关氮元素化学用语正确的是( )
A、氮分子的结构式: |
B、氮原子最外层的电子云图: |
C、NH3的比例模型: |
D、氮原子的轨道表示式: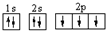 |
下列叙述正确的是( )
| A、工业上电解熔融的Al2O3冶炼铝用铁做阳极 |
| B、用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2 |
| C、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成2 molNaOH |
| D、用惰性电极电解CuSO4溶液一段时间后,加入CuO固体可以使CuSO4溶液恢复原来浓度 |
几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、T、Q的氢化物常态下均为无色气体 |
| B、L、M的单质与稀盐酸反应速率:M>L |
| C、R的氧化物对应的水化物可能具有两性 |
| D、L、Q形成的简单离子核外电子数相等 |
某元素的原子L层电子数比M层电子数多5个,该元素的最高正化合价为( )
| A、+3 | B、+4 | C、+5 | D、+6 |

 .
.