题目内容
16.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以测定某品牌茶叶中钙元素的质量分数并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如下操作:
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
①酒精灯 ②蒸发皿 ③坩埚 ④铁架台 ⑤三脚架 ⑥泥三角
(2)用KMnO4标准溶液滴定C溶液时所发生的反应的离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.此步操作过程中一定需要用到下列哪些仪器如图1(填写序号)B、C、D;

(3)达到滴定终点时的现象是无色变为紫色且半分钟内不褪色;
(4)滴定到终点,静置后,如图2读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将偏高 (填“偏高”、“偏低”、“无影响”).
(5)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是KSCN溶液,溶液呈红色.
(6)根据以上数据计算该茶叶样品中钙元素的质量分数为0.2%.
分析 (1)高温灼烧物质通常在坩埚内进行,据此选择;
(2)用KMnO4标准溶液滴定C溶液时所发生的反应为酸性溶液中高锰酸钾溶液氧化草酸生成二氧化碳;根据配制一定物质的量浓度的溶液方法及滴定操作方法选择使用的仪器;
(3)根据滴定结束前溶液为为无色,滴定结束时高锰酸钾溶液溶液过量进行解答;
(4)俯视液面导致滴定管中读数偏小,读出的高锰酸钾溶液体积偏小,计算出的钙离子消耗的草酸根离子物质的量偏大,测定结果偏高;
(5)根据检验铁离子遇到硫氰根离子溶液显示红色进行解答;
(6)根据滴定消耗高锰酸钾的物质的量计算出与钙离子反应剩余的草酸根离子的物质的量,再根据醋酸铵的总的质量及样品质量计算出钙离子的质量分数,注意滴定体积与样品体积的关系.
解答 解:(1)高温灼烧物质通常在坩埚内进行,要用到酒精灯、坩埚、泥三角、三脚架等,不需要用到的仪器有②蒸发皿,④铁架台,
故答案为:②④;
(2)用KMnO4标准溶液滴定C溶液时所发生的反应为酸性溶液中高锰酸钾溶液氧化草酸生成二氧化碳,反应的离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;将滤液C稀释至500mL时需要使用到容量瓶,滴定操作中需要使用滴定管和锥形瓶,即B、C、D正确,
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;B、C、D;
(3)滴定结束之前溶液为无色,滴定结束时高锰酸钾溶液过量,溶液变为紫色,所以滴定终点颜色变化为:无色变为紫色且半分钟内不褪色,
故答案为:无色变为紫色且半分钟内不褪色;
(4)滴定到终点,静置后,如图3读取KMnO4标准溶液的刻度数据,导致读数偏小,计算出的消耗的高锰酸钾溶液体积偏高,计算出的钙离子消耗的草酸根离子物质的量偏高,则测定的钙元素含量将偏高,
故答案为:偏高;
(5)滤液A中含有铁离子,可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,方法为:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素,
故答案为:KSCN溶液,溶液呈红色;
(6)7.44g草酸铵的物质的量为:$\frac{7.44g}{124g/mol}$=0.06mol,根据反应5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O可知与钙离子反应的草酸根离子的物质的量为:0.06mol-$\frac{5}{2}$×(0.10mol•L-1×0.01L)×$\frac{500ml}{25ml}$=0.01mol,根据化学式CaC2O4可知钙离子的物质的量为0.01mol,所以样品中钙离子的质量分数为:$\frac{40g/mol××0.01mol}{200g}$×100%=0.2%,
故答案为:0.2%.
点评 本题考查了探究茶叶中铁元素、钙元素的含量的方法及性质实验方案的设计,题目难度较大,注意掌握性质实验方案的设计方法,明确探究物质组成及含量的方法,试题培养了学生灵活应用所学知识解决实际问题的能力.

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸馏、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
| A. | 四个C-H键完全相同 | B. | CH4的一氯代物只有一种 | ||
| C. | CH2Cl2只有一种空间结构 | D. | 在常温常压下CH2Cl2为液体 |
| A. | SO2可以使溴水褪色,所以SO2具有漂白性 | |
| B. | 因为氢氧化铁胶体具有吸附性,所以常用于净水 | |
| C. | 因为液态HCl不导电,所以HCl是非电解质 | |
| D. | NH3的水溶液可以导电,所以NH3是电解质 |
| A. | 测量溶液的温度计要一直插在溶液中 | |
| B. | 应该向酸(碱)中慢慢滴加碱(酸) | |
| C. | 反应前需要用温度计测量酸(碱)温度 | |
| D. | 反应中酸或碱应适当过量 |
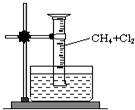 某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了如下实验.请填写下列空白: .
.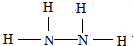 .
.