题目内容
5.金刚烷胺可用于治疗A型流感病毒,其结构简式及合成路线图如下,下列说法正确的是( )[尿素的分子式为CO(NH2)2]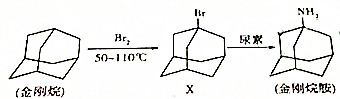
| A. | 金刚烷是不饱和烃 | B. | 金刚烷胺的分子式为C10H16N | ||
| C. | 上述反应都属于取代反应 | D. | X与尿素反应的另-种生成物是H2O |
分析 A.含有碳碳双键、碳碳三键的烃以及芳香烃属于不饱和烃;
B.键线式中交点、端点为碳原子,用H原子饱和碳的四价结构;
C.金刚烷中H原子被溴原子取代生成X,X中溴原子被-NH2取代生成金刚烷胺;
D.X与尿素反应的另-种生成物是COBr2.
解答 解:A.金刚烷中不含碳碳双键、碳碳三键,不是不饱和烃,金刚烷中只含有单键,属于饱和烃,故A错误;
B.由金刚烷胺的结构简式,可知分子式为C10H17N,故B错误;
C.金刚烷中H原子被溴原子取代生成X,X中溴原子被-NH2取代生成金刚烷胺,均属于取代反应,故C正确;
D.X与尿素发生取代反应生成金刚烷胺,另一种生成物是COBr2,故D错误.
故选:C.
点评 本题考查有机物的结构与性质,是有机化学基础常考题型,侧重考查学生分析与知识迁移应用能力,注意对基础知识的理解掌握.

练习册系列答案
相关题目
20.如图有关实验原理、操作或现象不正确的是( )
| A. | 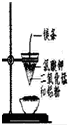 可制得金属锰,用同样的装置可制得金属铬 | |
| B. |  制取少量氨气 | |
| C. | 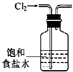 除去Cl2中的少量HCl | |
| D. |  制乙酸乙酯 |
1.分子式为C7H16,分子中含有三个甲基(-CH3)的同分异构体的数目是( )
| A. | 5 | B. | 4 | C. | 3 | D. | 2 |
8.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 将煤通过物理变化气化后再作为能源,可减少PM2.5引起的危害 | |
| B. | 普通玻璃属于无机非金属材料,有机玻璃属于新型无机非金属材料 | |
| C. | 在某爆炸事故救援现场,消防员发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭 | |
| D. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 |
5.下列实验装置或操作能达到实验目的是( )
| A. |  实验室制硝基苯 | B. | 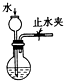 检查装置气密性 | ||
| C. |  利用排空气法收集丙烷 | D. | 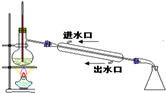 石油分馏 |
 某化学兴趣小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
某化学兴趣小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.