题目内容
19.食品安全一直是社会关注的话题.过氧化苯甲酰(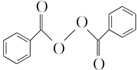 )过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图:
)过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图: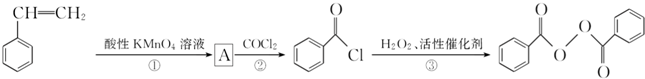
苯乙烯
请回答下列问题:
(1)A的结构简式为
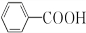 ;②的反应类型为取代反应.
;②的反应类型为取代反应.(2)写出反应③的化学方程式:
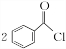 +H2O2$\stackrel{活性催化剂}{→}$
+H2O2$\stackrel{活性催化剂}{→}$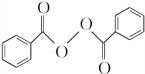 +2HCl;过氧化苯甲酰在酸性条件下水解的化学方程式为
+2HCl;过氧化苯甲酰在酸性条件下水解的化学方程式为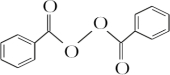 +2H2O$\stackrel{H+}{→}$
+2H2O$\stackrel{H+}{→}$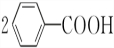 +H2O2.
+H2O2.(3)下列有关苯乙烯的说法正确的是ABC(填字母序号).
A.苯乙烯能使溴水褪色
B.苯乙烯存在一种同分异构体,其一氯代物仅有一种
C.苯乙烯分子中8个碳原子可能共平面
D.苯乙烯、庚烷燃烧耗氧量肯定相等
(4)苯甲酰氯(
 )能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称:苯甲酸乙酯.
)能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称:苯甲酸乙酯.(5)写出一个符合下列要求的过氧化苯甲酰的同分异构体的结构简式
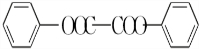 (或
(或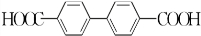 或
或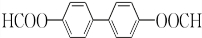 .
.①分子中不含碳碳双键或叁键;②分子中只含有一种含氧官能团;③核磁共振氢谱有3组峰,其峰面积之比为1:2:2.
分析 苯乙烯被酸性高锰酸钾溶液氧化生成A,A为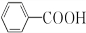 ,A先发生取代反应生成
,A先发生取代反应生成 ,以此解答(1)(2);
,以此解答(1)(2);
(3)苯乙烯具有碳碳双键和苯环,具有烯烃和苯的性质,能发生氧化反应、加成反应、加聚反应、取代反应,苯、乙烯中所有原子都共面;
(4)苯甲酰氯和水发生取代反应生成苯甲酸,苯甲酰氯和乙醇发生取代反应生成苯甲酸乙酯;
(5)过氧化苯甲酰同分异构体符合下列条件:
①分子中不含碳碳双键或叁键;②分子中只含有一种含氧官能团羧基或酯基;
③核磁共振氢谱有3组峰,说明含有3类氢原子,其峰面积之比为1:2:2,说明三种氢原子个数之比为1:2:2.
解答 解:苯乙烯被酸性高锰酸钾溶液氧化生成A,A为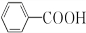 ,A先发生取代反应生成
,A先发生取代反应生成 ,
,
(1)A的结构简式为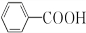 ,苯甲酸和酰氯发生取代反应生成苯甲酰氯,故答案为:
,苯甲酸和酰氯发生取代反应生成苯甲酰氯,故答案为: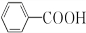 ;取代反应;
;取代反应;
(2)苯甲酰氯和双氧水发生取代反应生成过氧化苯甲酰,该反应③的化学方程式为 +H2O2$\stackrel{活性催化剂}{→}$
+H2O2$\stackrel{活性催化剂}{→}$ +2HCl,过氧化苯甲酰在酸性条件下水解生成苯甲酸,反应方程式为
+2HCl,过氧化苯甲酰在酸性条件下水解生成苯甲酸,反应方程式为 +2H2O$\stackrel{H+}{→}$
+2H2O$\stackrel{H+}{→}$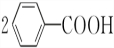 +H2O2,
+H2O2,
故答案为: +H2O2$\stackrel{活性催化剂}{→}$
+H2O2$\stackrel{活性催化剂}{→}$ +2HCl;
+2HCl;  +2H2O$\stackrel{H+}{→}$
+2H2O$\stackrel{H+}{→}$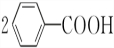 +H2O2;
+H2O2;
(3)A.苯乙烯中含有碳碳双键,所以能和溴发生加成反应而能使溴水褪色,故正确;
B.苯乙烯存在一种同分异构体 ,只有一种氢原子,所以其一氯代物仅有一种,故B正确;
,只有一种氢原子,所以其一氯代物仅有一种,故B正确;
C.苯、乙烯中的所有原子共面,且二者直接相连,所以苯乙烯分子中8个碳原子可能共平面,故正确;
D.苯乙烯、庚烷分子式分别是C8H8、C8H18,二者的物质的量未知,所以无法计算燃烧耗氧量是否相等,故错误;
故选ABC;
(4)苯甲酰氯和水发生取代反应生成苯甲酸,是氯原子被-OH取代,苯甲酰氯中氯原子被乙醇中的CH3CH2O-取代,所以和乙醇发生取代反应生成苯甲酸乙酯,
故答案为:苯甲酸乙酯;
(5)过氧化苯甲酰同分异构体符合下列条件:
①分子中不含碳碳双键或叁键;②分子中只含有一种含氧官能团羧基或酯基;
③核磁共振氢谱有3组峰,说明含有3类氢原子,其峰面积之比为1:2:2,说明三种氢原子个数之比为1:2:2,符合条件的同分异构体为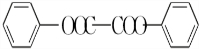 (或
(或 或
或 ,
,
故答案为: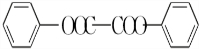 (或
(或 或
或 .
.
点评 本题考查有机物推断,侧重考查学生分析判断能力,根据反应前后结构简式变化确定反应类型,难点是(5)题同分异构体种类判断,易错点是(3)B中立方烷和苯乙烯属于同分异构体,题目难度中等.

| A. | 地沟油和矿物油都属于酯类物质 | |
| B. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化 | |
| D. | 蛋白质、棉花、淀粉、油脂都是由高分子组成的物质 |
| A. | 4.6克钠与水反应时失去的电子数目为0.2NA | |
| B. | 1 L0.5mol•L-1 Na2SO4溶液中所含有的Na+离子数日为NA | |
| C. | 在标准状况下,22.4LNH3所含的氨分子数目为NA | |
| D. | 常温常压下2克氢气所含原子数日为NA |
| A. | 石油的分馏、煤的干馏、电解质溶液导电均属于物理变化 | |
| B. | 做衣服的棉、麻、蚕丝的主要成分都是纤维素 | |
| C. | 鸡蛋清中加人胆矾可以使蛋白质发生聚沉.加水后重新溶解 | |
| D. | 乙烯和氯乙烯都可以通过加聚反应得到高分子化合物 |
| A. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| B. | 近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| C. | 食品保鲜膜、一次性食品袋的主要成分是聚乙烯 | |
| D. | 使用纤维素和淀粉为原料制成的微生物降解塑料,可治理“白色污染” |
| A. | 碱性溶液:Cu2+、Fe3+、NO3-、SO42- | |
| B. | 加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- | |
| C. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| D. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |

已知:①2NO+Na2O2=2NaNO2;
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(1)加热装置A前,先通一段时间N2,目的是排除装置中的空气.
(2)装置A中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.实验结束后,将B瓶中的溶液经蒸发浓缩、冷却结晶(填操作名称)、过滤可获得CuSO4•5H2O.
(3)仪器C的名称为干燥管,其中盛放的药品为碱石灰(填名称).
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,加入稀硫酸溶液中有气泡产生且在试管口上方出现红棕色气体,则产物是NaNO2(注明试剂、现象).
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%.
(6)设计合理实验比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2的电离程度相对大小.(简要说明实验步骤、现象和结论,仪器和药品自选)
25°C.
| A. | 氧化铝是一种高硬度、高熔沸点的化合物 | |
| B. | 铝是活泼的金属,其合金抗腐蚀能力差 | |
| C. | 铝合金具有密度小、高强度及较好的可塑性 | |
| D. | 铝合金可用于制飞机骨架等 |
 .
.