题目内容
已知:正四面体形分子E和直线形分子G反应,生成四面体形分子L和直线形分子M(组成E分子的元素的原子序数均小于10,组成G分子的元素为第三周期元素)。
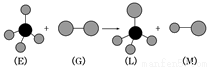
下列判断中正确的是
A.常温常压下,L是一种液态有机物
B.E的二溴代物只有一种结构
C.G具有强氧化性和漂白性
D.上述反应的类型是加成反应
B
【解析】
试题分析:由已知条件,E为甲烷,G为氯气,L为一氯甲烷,M为氯化氢,A、常温常压下,一氯甲烷为气体,A错误;B、甲烷为正四面体结构,二溴代物只有一种,B正确;C、氯气具有强氧化性,不具有漂白性,C错误;D、甲烷与氯气的反应为取代反应,D错误;答案选B。
考点:甲烷的取代反应

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案(13分)有A、B、C、D、E五种元素,其相关信息如下:
元素 | 相关信息 |
A | A原子的1s轨道上只有1个电子 |
B | B是电负性最大的元素 |
C | C基态原子的2p轨道中有3个未成对电子 |
D | D是主族元素且与E同周期,其最外能层上有2个运动状态不同的电子 |
E | E的+1价离子的M能层中所有能级各轨道都有电子且没有未成对电子 |
请回答下列问题:
(1)写出元素E的基态原子的电子排布式_________________。
(2)CA3分子中C原子的杂化类型是________;在元素E的硫酸盐溶液中逐渐通入CA3,可以观察到的实验现象是 ,发生的有关反应的离子方程式为 。
(3)C与A还可形成C2A4、CA5等化合物,二者都能与盐酸反应。则C2A4与盐酸反应的离子方程式为 。CA5还可与水反应产生无色气体,且所得溶液显碱性,则CA5的电子式为 ,与水反应的化学方程式 。
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有____(填序号);
1mol该离子中含有 个σ键。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_________(填序号)。
a.平面正方形 B.正四面体 c.三角锥形 D.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示。
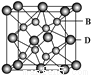
其中D离子的配位数为 ________,该晶体的化学式为__________。
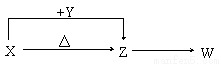
 2AB(气)达到平衡的标志是
2AB(气)达到平衡的标志是 
