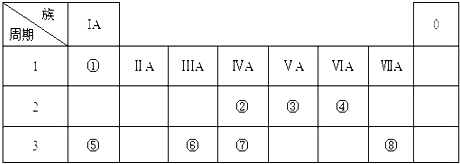
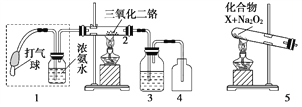
题目内容
【题目】将0.1mol下列物质置于1L水中充分搅拌后,溶液中阴离子数最多的是( )
A.KCl
B.Mg(OH)2
C.Na2CO3
D.MgSO4
【答案】C
【解析】解:对于A和D,由于KCl和MgSO4溶于水并完全电离,所以n(Cl﹣)=n(SO42﹣)=0.1mol l(水电离出的OH﹣可忽略);对于B,B中的Mg(OH)2在水中难溶,故溶液中n(OH﹣)<0.1mol;对于C,在Na2CO3溶液中,由于CO32﹣+H2OHCO3﹣+OH﹣ , 阴离子数目会增加,即阴离子物质的量大于0.1mol.由上分析,Na2CO3溶液中的阴离子数目最多,C项正确.故答案为C.
根据盐类的水解和物质的溶解度思考.

【题目】某学习小组利用图1装置进行CO2与饱和Na2CO3溶液反应制备NaHCO3 . 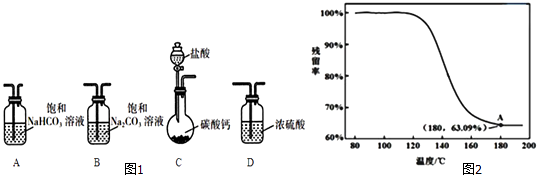
(1)选取必要的实验装置,正确的连接顺序为(填序号).
(2)为确定制得的固体样品是纯净的NaHCO3 , 小组同学提出下列实验方案:甲方案:将样品溶液与饱和澄清石灰水反应,观察现象.
乙方案:将样品溶液与BaCl2溶液反应,观察现象.
丙方案:测定pH法.
丁方案:热重分析法.
①判定甲方案(填“可行”或“不可行”).
②为判定乙方案的可行性,某同学用纯净的NaHCO3配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
NaHCO3溶液 | 0.2molL﹣1 | 0.1molL﹣1 | 0.02molL﹣1 |
0.2molL﹣1 | 浑浊 | 浑浊 | 少许浑浊 |
0.1molL﹣1 | 浑浊 | 少许浑浊 | 无现象 |
0.02molL﹣1 | 少许浑浊 | 无现象 | 无现象 |
(i)此实验已可说明乙方案是不可行的.请结合以下数据,并通过计算说明产生浑浊的原因.
[己知:0.l molL﹣1 NaHCO3溶液电离出的c(CO32﹣)为0.001lmolL﹣1 , Ksp(BaCO3)=5.1×10﹣9]
答: .
(ii)产生浑浊(伴有气体产生)的离子方程式 .
③用pH计测定的丙方案如下:
取m克的固体样晶溶解于水配成V mL的溶液,用pH计测pH:
还应补充的实验是:
④进行丁方案实验,得到固体残留率随温度变化的曲线如图2所示,根据A点坐标得到的结沦是 .
(残留率= ![]() ×100%)
×100%)