题目内容
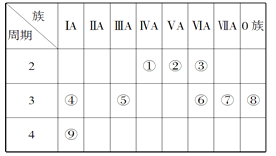
【题目】下表为元素周期表的一部分,请参照元素①﹣⑧在表中的位置,用化学用语回答下列问题: 
(1)④、⑤、⑥的原子半径由大到小的顺序为 .
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是 .
(3)③的气态氢化物的电子式 .
(4)⑤的最高价氧化物对应水化物的溶液与单质⑥、单质⑧分别反应的离子方程式、 .
(5)单质①在单质⑧中燃烧,火焰为色.
【答案】
(1)Na>Al>O
(2)HClO4>H2CO3>H2SiO3
(3)![]()
(4)2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
(5)苍白
【解析】解:由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl,(1)电子层越多半径越大,所以Na、Al>O,电子层一样多的原子,核电荷数越多半径越小,即Na>Al,所以答案是:Na>Al>O;(2)非金属性Cl>C>Si,则最高价含氧酸的酸性由强到弱的顺序是HClO4>H2CO3>H2SiO3 , 所以答案是:HClO4>H2CO3>H2SiO3;(3)③的气态氢化物为氨气,其电子数为 ![]() ,所以答案是:
,所以答案是: ![]() ;(4)Al与NaOH溶液反应生成偏铝酸钠和氢气,离子反应为2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;氯气与NaOH溶液反应生成氯化钠、次氯酸钠,离子反应为Cl2+2OH﹣=Cl﹣+ClO﹣+H2O; 所以答案是:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(5)单质①在单质⑧中燃烧,生成HCl,火焰为苍白色,所以答案是:苍白.
;(4)Al与NaOH溶液反应生成偏铝酸钠和氢气,离子反应为2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;氯气与NaOH溶液反应生成氯化钠、次氯酸钠,离子反应为Cl2+2OH﹣=Cl﹣+ClO﹣+H2O; 所以答案是:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(5)单质①在单质⑧中燃烧,生成HCl,火焰为苍白色,所以答案是:苍白.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目