��Ŀ����
����Ŀ��ij��ȤС������ͼװ��̽�����Ĵ�������
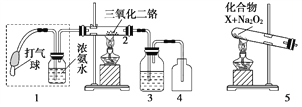
(1)���������Ļ�ѧ����ʽΪ____________________________________��
(2)���Ȳ�����2һ��ʱ���ѹ1�д��������������۲쵽2�����ʳʺ���״̬��ֹͣ���Ⱥ����ܱ��ֺ��ȣ��÷�Ӧ��________��Ӧ(����ȡ����ȡ�)��
(3)Ϊ��֤��װ��4�н��۲쵽����ɫ���壬װ��3Ӧװ��________����ȡ��3����4�н��۲쵽�������̣�ԭ����___________________________________��
(4)Ϊʵ�ְ���������Ҳ����װ��5�滻װ��________(��װ�ô���)��������XΪ________(ֻдһ��)��Na2O2��������_____________________________��
���𰸡� 4NH3��5O2![]() 4NO��6H2O ���� ŨH2SO4 ���ɵ�NO��O2��Ӧ����NO2��NO2��ˮ��Ӧ����HNO3��NH3��HNO3��Ӧ������NH4NO3 1 NH4Cl ��HCl��Ӧ��������(�����𰸾�����)
4NO��6H2O ���� ŨH2SO4 ���ɵ�NO��O2��Ӧ����NO2��NO2��ˮ��Ӧ����HNO3��NH3��HNO3��Ӧ������NH4NO3 1 NH4Cl ��HCl��Ӧ��������(�����𰸾�����)
�������������������1��NH3��O2�ڴ�������������NO��ˮ����ѧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
��2���÷�ӦΪ���ȷ�Ӧ�����Բ����Ⱥ����ܱ��ֺ���״̬��
��3�����Ĵ�����������Ҫ�Ʊ�NH3��O2���ɵó�װ��1���������Ʊ�NH3��O2����װ��2��NH3��O2�ڴ��������������£���Ӧ����NO��H2O������װ��3��ȥH2O��δ��Ӧ��NH3����װ��4��NO������ΪNO2����Ũ���Ὣ������ȥ������װ��3Ӧװ��Ũ���������ȥ���������ɵ�NO��O2��Ӧ����NO2,NO2��ˮ��Ӧ����HNO3,�ӷ�����NH3��HNO3��Ӧ������NH4NO3���������̡�
��4��װ��5��1���ɲ���NH3������Ϊʵ�ְ��Ĵ�����,Ҳ����װ��5�滻װ��1��NH4Cl���ȷֽ�ɵ�NH3��HCl����HCl��Na2O2������O2�����Ի�����XΪNH4Cl��Na2O2����������NH4Cl���ȷֽ�IJ���HCl��Ӧ����������

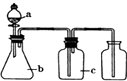
����Ŀ���±���a��b��c��ʾ��Ӧ�����м��˵��Լ���������ͼװ����ȡ���������ռ��������ǣ� ��
��� | ���� | a | b | c |
|
A | NH3 | Ũ��ˮ | ��ʯ�� | ��ʯ�� | |
B | CO2 | ���� | ̼��� | ����NaHCO3��Һ | |
C | NO | ϡ���� | ͭм | H2O | |
D | Cl2 | Ũ���� | �������� | ����NaCl��Һ |
A.A
B.B
C.C
D.D