题目内容
1.下列离子方程式正确的是( )| A. | 铁与过量稀硝酸反应:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O | |
| B. | 将铜与硫单质混合加热:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| C. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
分析 A、稀硝酸是氧化性酸,当硝酸过量时,将铁氧化为Fe3+;
B、硫只能将铜氧化为+1价;
C、NaHCO3只能拆为钠离子和HCO3-;
D、氢氧化铁的溶解度小于氢氧化镁.
解答 解:A、稀硝酸是氧化性酸,当硝酸过量时,将铁氧化为Fe3+,故离子方程式为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,故A错误;
B、硫只能将铜氧化为+1价,故铜和硫反应后生成Cu2S,反应为:2Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$Cu2S,故B错误;
C、NaHCO3只能拆为钠离子和HCO3-,故离子方程式为:HCO3-+H+=H2O+CO2↑,故C错误;
D、氢氧化铁的溶解度小于氢氧化镁,故氢氧化镁可以和铁离子反应转化为氢氧化铁沉淀,离子方程式为:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+,故D正确.
故选D.
点评 本题考查离子方程式书写原则的分析,正误判断方法,注意电荷守恒,原子守恒的应用,题目难度中等.

练习册系列答案
相关题目
11.下列说法正确的是( )
| A. | 焓减小的反应通常是自发的,能够自发进行的反应都是焓减小的反应 | |
| B. | 熵增加的反应通常是自发的,能够自发进行的反应都是熵增加的反应 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | △H<0且△S<0的反应一定能自发发生 |
12.下列热化学方程式正确的是(△H的绝对值均正确)( )
| A. | 2NO2═O2+2NO;△H=+116.2kJ/mol(燃烧热) | |
| B. | 2S(s)+2O2(g)═2SO2(g);△H=-269.8kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| D. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) |
9.在同温同压下,A容器中盛有H2,B容器中盛有NH3,它们所含的原子总数相等,则两容器中气体的密度之比为( )
| A. | 2:1 | B. | 1:2 | C. | 2:3 | D. | 2:17 |
6.中国南海海域是全球范围内石油储量与可开采储量较丰富、开采潜力较大的地方,有“第二个波斯湾”之称.下列关于石油的说法正确的是( )
| A. | 石油属于可再生矿物能源 | B. | 石油只含有碳、氢、氧三种元素 | ||
| C. | 将原油通过萃取、分液可获得汽油 | D. | 石油分馏所得的各馏分仍是混合物 |
10.设 N A代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 2.3 g 金属钠所含钠原子数目为0.2 N A | |
| B. | 2 g 氢气所含原子数目为2 N A | |
| C. | 17 g NH 3所含的分子数为2 N A | |
| D. | N A个O 2和 N A个H 2的所含原子数目比等于16:1 |
11.下列化学变化涉及的反应类型为加成反应的是( )
| A. | 苯→溴苯 | B. | 苯→硝基苯 | C. | 乙烯→氯乙烷 | D. | 乙醇→乙酸乙酯 |
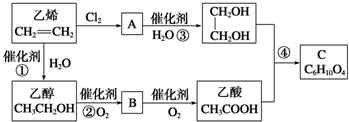
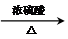 CH3COOCH2-CH2OOCCH3+2H2O.
CH3COOCH2-CH2OOCCH3+2H2O. ;B分子中有6个原子共面,结构简式为CH2=CH2.
;B分子中有6个原子共面,结构简式为CH2=CH2.