题目内容
已知反应A2(g)+2B2(g)?2AB2(g)△H>0,下列说法正确的是( )
| A、升高温度正反应速率加快,逆反应速率减慢 |
| B、0.1mol A2和0.2mol B2反应达到平衡时生成0.2mol AB2 |
| C、达平衡后,升高温度,B的转化率增大 |
| D、催化剂可同等程度地改变正、逆反应速率 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、升高温度,正逆反应速率均加快;
B、可逆反应不能进行彻底;
C、升高温度,化学平衡向着吸热方向进行;
D、催化剂可以同等程度地改变正、逆反应速率.
B、可逆反应不能进行彻底;
C、升高温度,化学平衡向着吸热方向进行;
D、催化剂可以同等程度地改变正、逆反应速率.
解答:
解:A、升高温度,可以使所以反应的正逆反应速率加快,但是加快的程度不一样,故A错误;
B、可逆反应不能进行彻底,所以.1mol A2和0.2mol B2反应达到平衡时生成AB2的量会小于0.2mol,故B错误;
C、升高温度,化学平衡向着吸热方向进行,即正向进行,所以B的转化率增大,故C正确;
D、催化剂的催化特点:可以同等程度地改变正、逆反应速率,故D正确.
故选CD.
B、可逆反应不能进行彻底,所以.1mol A2和0.2mol B2反应达到平衡时生成AB2的量会小于0.2mol,故B错误;
C、升高温度,化学平衡向着吸热方向进行,即正向进行,所以B的转化率增大,故C正确;
D、催化剂的催化特点:可以同等程度地改变正、逆反应速率,故D正确.
故选CD.
点评:本题考查学生影响化学反应速率、平衡移动的因素等知识,注意催化剂的催化特点:可以同等程度地改变正、逆反应速率,不会引起平衡移动.

练习册系列答案
相关题目
20mL 0.1mol/L溶液中含有Fe2+,向其中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得沉淀和滤液.已知:Kaq=[Fe(OH)3]=4.0×10-38,Kaq=[Fe(OH)2]=8.0×10-16.( )
| A、沉淀中只有Fe(OH)3 |
| B、沉淀中有Fe(OH)3和Fe(OH)2 |
| C、滤液c(Fe3+)=4.0×10-8mol/L |
| D、向滤液中滴加FeCl2溶液,无沉淀产生 |
有aXm+和bYn-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A、b-a=n+m |
| B、a-b=n+m |
| C、核电荷数Y=X |
| D、核电荷数Y>X |
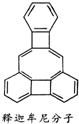 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),其结构简式如图所示.有关该有机分子的下列说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),其结构简式如图所示.有关该有机分子的下列说法正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有22个碳原子和22个氢原子 |
| D、该有机物的一氯代物只有3种 |
下列描述的一定是金属元素的是( )
| A、易失去电子的物质 |
| B、能与酸反应的物质 |
| C、原子最外电子层只有一个电子的元素 |
| D、原子核内有11个质子的元素 |
合成氨工业生产中所用的α-Fe催化剂的成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时混合物中铁的质量分数约为( )
| A、70.0% |
| B、77.8% |
| C、72.4% |
| D、75.0% |
下列关于能源和作为能源物质的叙述中错误的是( )
| A、燃料燃烧时将化学能全部转化为热能 |
| B、绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C、物质的化学能可以在不同条件下转为热能、电能为人类所利用 |
| D、化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
下列叙述正确的是( )
| A、金属氧化物均为碱性氧化物 |
| B、酸性氧化物均为非金属氧化物 |
| C、熔融态能导电的物质是电解质 |
| D、一定条件下电解质能电离为离子 |
已知某镍镉(Ni-Cd)可充电电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
| ||
| 充电 |
| A、放电时Cd电极发生氧化反应 |
| B、放电时电解质溶液中的OH-向负极移动 |
| C、放电时负极附近溶液的碱性不变 |
| D、充电时阳极反应:Ni(OH)2+OH-+e-═NiOOH+H2O |