题目内容
16.物质A在一定条件下加热分解:2A→B(g)+2C(g)+4D(g)(g表示气态),生成物均为气体,若A的相对分子质量为77,则A完全分解后所得混合气体的平均相对分子质量是( )| A. | 11 | B. | 22 | C. | 44 | D. | 77 |
分析 假设A为2mol,由方程式可知生成B、C、D总物质的量为1mol+2mol+4mol=7mol,根据质量守恒定律可知混合物质量等于A的质量,再根据$\overline{M}$=$\frac{{m}_{总}}{{n}_{总}}$计算.
解答 解:假设A为2mol,由方程式可知生成B、C、D总物质的量为1mol+2mol+4mol=7mol,根据质量守恒定律可知混合物质量等于A的质量,故混合气体总质量为2mol×77g/mol=154g,则混合气体平均相对分子质量为$\frac{154}{7}$=22,故选:B.
点评 本题考查化学方程式计算,难度不大,注意利用赋值法简化计算.

练习册系列答案
相关题目
6.下列叙述中正确的是( )
| A. | SiO2和NO2能与强碱溶液反应,都是酸性氧化物 | |
| B. | 不锈钢材料因含有铬、镍所以抗腐蚀性好 | |
| C. | 普通玻璃、钢化玻璃、玻璃钢都属于硅酸盐产品,水玻璃可用于木材防腐 | |
| D. | MgO和A12O3熔点较高都可以做耐火材料,都能和强碱溶液反应 |
7.V L含有(NH4)2SO4和K2SO4的混合溶液,已知NH4+浓度为amol•L-1,SO42-浓度为bmol•L-1.则原混合溶液中钾离子的物质的量浓度为( )
| A. | (b-2a)bmol•L-1 | B. | $\frac{(b-2a)}{2}$bmol•L-1 | C. | (2b-a)bmol•L-1 | D. | $\frac{(2b-a)}{2}$bmol•L-1 |
4.下列有关化学用语的表示正确的是( )
| A. | 四氯化碳分子的电子式: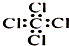 | B. | 对硝基甲苯的结构简式: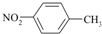 | ||
| C. | 羟基的电子式: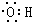 | D. | 乙醛的结构简式:CH3COH |
11.将1.76g铜镁合金完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1344mL(标准状况),向反应后的溶液中加入1.0mo1•L-1NaOH溶液,当金属离子全部沉淀时,得到3.12g沉淀.下列说法不正确的是(写出过程)( )
| A. | 该合金中铜与镁的物质的量之比是1:1 | |
| B. | 该浓硝酸中HN03的物质的量浓度是14.0mo1•L-1 | |
| C. | NO2和N2O4的混合气体中,NO2的体积分数是80% | |
| D. | 得到3.12g沉淀时,加入NaOH溶液的体积是620mL |
13.丙酮和苯酚都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如图:
相关化合物的物理常数
回答下列问题:
(1)反应①和②分别在装置A和C中进行(填装置符号).
(2)反应②为放热(填“放热”或“吸热”)反应.反应温度控制在50-60℃,温度过高的安全隐患是温度过高会导致爆炸.
(3)在反应器A中通入的X是氧气或空气.
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂,优点是用量少,缺点是腐蚀设备.
(5)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚.
(7)用该方法合成苯酚和丙酮的优点是原子利用率高.

相关化合物的物理常数
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 苯酚 | 94 | 1.0722 | 182 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 异丙苯 | 120 | 0.8640 | 153 |
(1)反应①和②分别在装置A和C中进行(填装置符号).
(2)反应②为放热(填“放热”或“吸热”)反应.反应温度控制在50-60℃,温度过高的安全隐患是温度过高会导致爆炸.
(3)在反应器A中通入的X是氧气或空气.
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂,优点是用量少,缺点是腐蚀设备.
(5)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚.
(7)用该方法合成苯酚和丙酮的优点是原子利用率高.
14.三氯化磷(PCl3)是一种重要的有机合成催化剂.实验室常用红磷与干燥的Cl2制取PCl3,装置如图1所示.

已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl.PCl3、POCl3的熔沸点见表.
请答下面问题:
(1)B中所装试剂是浓硫酸,F中碱石灰的作用是吸收多余的Cl2,防止空气中的水蒸气进入烧瓶与PCl3反应.
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行.通干燥CO2的作用是排尽装置中的空气,防止红磷自燃,
(3)实验制得的粗产品中常含有POCl3、PCl5等.加入红磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是先关闭K1,打开K2,等B中溶液上方充满黄绿色气体后,打开K1,关闭K2.
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X.某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象.
(6)玻璃管之间的连接需要用到胶皮管,连接的方法是:先把把玻璃管口用水润湿,然后稍稍用力即可把玻璃管插入橡皮管.甲同学将装置A的示意图画成图2,该示意图中明显的错误是没有(用酒精灯)加热.

已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl.PCl3、POCl3的熔沸点见表.
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)B中所装试剂是浓硫酸,F中碱石灰的作用是吸收多余的Cl2,防止空气中的水蒸气进入烧瓶与PCl3反应.
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行.通干燥CO2的作用是排尽装置中的空气,防止红磷自燃,
(3)实验制得的粗产品中常含有POCl3、PCl5等.加入红磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是先关闭K1,打开K2,等B中溶液上方充满黄绿色气体后,打开K1,关闭K2.
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X.某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象.
| 实验步骤 | 实验现象 | 实验结论 |
| ① | 溶液X中含有Na+ | |
| ② | 溶液X中含有Cl- |
 A、B、C、D、E五种物质所含元素均有两种相同,且焰色反应均为黄色,B比A相对更稳定,C、D是工业上重要的化工原料,也是实验室常用的药品,C、D在一定的条件下可以相互转化,F与A、B、C、D在一定条件下均可发生反应,它们的部分转化关系如图(部分反应物或生成物省略).
A、B、C、D、E五种物质所含元素均有两种相同,且焰色反应均为黄色,B比A相对更稳定,C、D是工业上重要的化工原料,也是实验室常用的药品,C、D在一定的条件下可以相互转化,F与A、B、C、D在一定条件下均可发生反应,它们的部分转化关系如图(部分反应物或生成物省略). ,C的俗名为火碱或烧碱;
,C的俗名为火碱或烧碱;