题目内容
在化学反应CO2+3H2?CH3OH+H2O中,下列措施中能使平衡混合物中
增大的是( )
| n(CH3OH) |
| n(CO2) |
| A、加入催化剂 |
| B、充入He(g),使体系压强增大 |
| C、将H2O(g)从体系中分离 |
| D、降低温度 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:要使平衡混合物中
增大,应使平衡向正反应方向移动,根据影响平衡移动的因素来回答判断.
| n(CH3OH) |
| n(CO2) |
解答:
解:使平衡混合物中
增大,应使平衡向正反应方向移动即可.
A.加入催化剂不会引起平衡的移动,故A错误;
B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,比值不变,故B错误;
C.将H2O(g)从体系中分离,平衡向正反应方法移动,比值增大,故C正确;
D.不知道反应的吸放热情况,所以降低温度,平衡的移动方向无法判断,比值变化也无法判断,故D错误.
故答案为:C.
| n(CH3OH) |
| n(CO2) |
A.加入催化剂不会引起平衡的移动,故A错误;
B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,比值不变,故B错误;
C.将H2O(g)从体系中分离,平衡向正反应方法移动,比值增大,故C正确;
D.不知道反应的吸放热情况,所以降低温度,平衡的移动方向无法判断,比值变化也无法判断,故D错误.
故答案为:C.
点评:本题考查平衡移动的问题,题目难度不大,注意平衡移动原理的理解和应用为解答该题的关键.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
一定温度下,向体积为2L的密闭容器中充入1mol PCl5(g),发生反应:PCl5(g)?PCl3(g)+Cl2(g)△H=+QKJ?mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示.下列说法正确的是( )


| A、0-3s内,容器中气体的压强不断增大 |
| B、达到平衡时放出0.6QkJ热量 |
| C、其他条件不变,升高温度,平衡常数减小 |
| D、其他条件不变,再向容器中充入1molPCl5(g),则达到平衡时,c(PCl5)>0.4mol?L-1 |
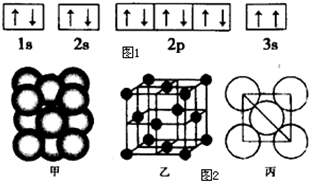 现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题. 根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.
根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.

 ,则该烃可能有2种.
,则该烃可能有2种.