题目内容
实验室需要200mL 0.4mol/L的碳酸钠溶液.
(1)需准确称量碳酸钠固体 g.
(2)必须用到的仪器是(填写序号) .
①100mL量筒 ②烧杯 ③100mL容量瓶 ④250mL容量瓶 ⑤天平和砝码⑥胶头滴管 ⑦玻璃棒
(3)若出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是 .
A.将已溶解的碳酸钠溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的碳酸钠溶液向容量瓶内转移时,因操作不当使部分溶液溅出瓶外
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切.
(1)需准确称量碳酸钠固体
(2)必须用到的仪器是(填写序号)
①100mL量筒 ②烧杯 ③100mL容量瓶 ④250mL容量瓶 ⑤天平和砝码⑥胶头滴管 ⑦玻璃棒
(3)若出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是
A.将已溶解的碳酸钠溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的碳酸钠溶液向容量瓶内转移时,因操作不当使部分溶液溅出瓶外
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切.
考点:溶液的配制
专题:实验题
分析:(1)依据n=c×V,m=n×M计算需要的碳酸钠的质量;
(2)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(3)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
(2)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(3)根据c=
| n |
| V |
解答:
解:(1)要配置200mL 0.4mol/L的碳酸钠溶液,需要选择250ml的容量瓶,需要碳酸钠的物质的量n=0.25L×0.4mol/L=0.1mol,其质量m=0.1mol×106g/mol=10.6g,
故答案为:10.6;
(2)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,
所以需要的仪器有:②烧杯 ④250mL容量瓶 ⑤天平和砝码⑥胶头滴管 ⑦玻璃棒,即必须用到的仪器是②④⑤⑥⑦;
故答案为:②④⑤⑥⑦;
(3)A.将已溶解的碳酸钠溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故A正确;
B.将烧杯内的碳酸钠溶液向容量瓶内转移时,因操作不当使部分溶液溅出瓶外,溶质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故B正确;
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,吸出的溶液中含有溶质,质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故C正确;
故答案为:A、B、C.
故答案为:10.6;
(2)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管,
所以需要的仪器有:②烧杯 ④250mL容量瓶 ⑤天平和砝码⑥胶头滴管 ⑦玻璃棒,即必须用到的仪器是②④⑤⑥⑦;
故答案为:②④⑤⑥⑦;
(3)A.将已溶解的碳酸钠溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故A正确;
B.将烧杯内的碳酸钠溶液向容量瓶内转移时,因操作不当使部分溶液溅出瓶外,溶质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故B正确;
C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切,吸出的溶液中含有溶质,质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小,故C正确;
故答案为:A、B、C.
点评:本题考查一定物质的量浓度溶液的配制,易错点是计算溶质的质量,注意容量瓶规格的选择和误差分析的方法.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
一定条件下,在容积为10L的密闭容器中,将l mol X和1mol Y进行如下反应:2X(g)+Y(g)?Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
| A、60 s内X的平均反应速率为0.001 mol?L-1?s-1 | ||
B、将容器的容积变为20 L,Z的新平衡浓度将等于原平衡浓度的
| ||
| C、若温度和体积不变,往容器内增加1 mol X,X的转化率将增大 | ||
| D、若升高温度,X的体积分数增大,则正反应的△H>0 |
 80℃时,将0.40molN2O4气体充入2L已经抽空的固定容积的密闭容器中发生反应:N2O4(g)?2NO2(g)△H>0,每隔一段时间对该容器内的物质进行分析,得到如下数据:
80℃时,将0.40molN2O4气体充入2L已经抽空的固定容积的密闭容器中发生反应:N2O4(g)?2NO2(g)△H>0,每隔一段时间对该容器内的物质进行分析,得到如下数据:
 三种元素形成的气态氢化物最稳定的是
三种元素形成的气态氢化物最稳定的是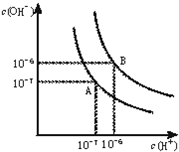 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.