题目内容
以下是有关SO2、CL
2的性质实验.
(1)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究SO2和CI2的性质.
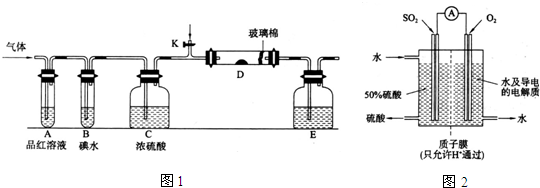
①若从左端分别通入SO2和Cl2,装置A中观察到的现象 (填“相同”或“不相同”);若装置D中装的V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 .
②SO2通入B中,溶液颜色褪去,则该反应的离子方程式为 .
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成.若向该试管中加入足量 (填字母),能产生白色沉淀.
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成价酸根离子X,X中S和O的质量比为2:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式: .
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图2,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触,.通入SO2的电极为 极,其电极反应式为 ;电池的总反应式为 .
2的性质实验.
(1)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究SO2和CI2的性质.

①若从左端分别通入SO2和Cl2,装置A中观察到的现象
②SO2通入B中,溶液颜色褪去,则该反应的离子方程式为
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成.若向该试管中加入足量
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成价酸根离子X,X中S和O的质量比为2:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式:
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图2,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触,.通入SO2的电极为
考点:氯、溴、碘的性质实验,探究二氧化硫与水和品红溶液的反应
专题:实验设计题
分析:(1)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性;SO2在V2O5作催化剂,加热可与O2反应生成SO3;
②SO2与I2能发生氧化还原反应;
(2)SO2在碱性条件下或被氧化成硫酸根,都与氯化钡能产生沉淀;
(3)x为SO32-,遇Cl2能被氧化成SO42-,据此答题;
(4)SO2来制备硫酸,SO2被氧化,作还原剂,据此判断电极和书写电极反应.
②SO2与I2能发生氧化还原反应;
(2)SO2在碱性条件下或被氧化成硫酸根,都与氯化钡能产生沉淀;
(3)x为SO32-,遇Cl2能被氧化成SO42-,据此答题;
(4)SO2来制备硫酸,SO2被氧化,作还原剂,据此判断电极和书写电极反应.
解答:
解:(1)①二氧化硫具有漂白性,氯气与水反应生成HClO,HClO具有漂白性,所以A中观察到的现象相同;SO2在V2O5作催化剂,加热可与O2反应生成SO3,化学方程式为
2SO2+O2
2SO3,故答案为:相同;2SO2+O2
2SO3;
②SO2与I2能发生氧化还原反应,从而使碘水颜色褪去,离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
(2)A.在试管里加入氨水后,二氧化硫与氨水反应生成亚硫酸铵,亚硫酸铵与氯化钡可生成亚硫酸钡白色沉淀,故A正确;
B.足量的SO2通入装有氯化钡溶液的试管,再加稀盐酸无沉淀产生,故B错误;
C.足量的SO2通入装有氯化钡溶液的试管,溶液呈酸性,硝酸钾中的硝酸根离子在酸性条件下,有强氧化性,可以将SO2氧化成硫酸根,再与氯化钡产生硫酸钡白色沉淀,故C正确;
D.硫化钠溶液与SO2反应产生硫单质,有淡黄色沉淀,故D错误;
故选AC;
(3)x为SO32-,遇Cl2能被氧化成SO42-,SO42-遇盐酸酸化的氯化钡溶液,有白色沉淀产生,Cl2氧化SO32-的离子方程式为Cl2+SO32-+H2O=SO42-+2Cl-+2H+,故答案为:Cl2+SO32-+H2O=SO42-+2Cl-+2H+;
(4)SO2来制备硫酸,SO2被氧化,作还原剂,所以SO2在负极反应,其电极反应式为SO2-2e-+2H2O=SO42-+4H+;SO2制备硫酸,O2作氧化剂,电池的总反应式为2SO2+O2+2H2O=2H2SO4,故答案为:负;SO2-2e-+2H2O=SO42-+4H+;2SO2+O2+2H2O=2H2SO4.
2SO2+O2
| 催化剂 |
| △ |
| 催化剂 |
| △ |
②SO2与I2能发生氧化还原反应,从而使碘水颜色褪去,离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
(2)A.在试管里加入氨水后,二氧化硫与氨水反应生成亚硫酸铵,亚硫酸铵与氯化钡可生成亚硫酸钡白色沉淀,故A正确;
B.足量的SO2通入装有氯化钡溶液的试管,再加稀盐酸无沉淀产生,故B错误;
C.足量的SO2通入装有氯化钡溶液的试管,溶液呈酸性,硝酸钾中的硝酸根离子在酸性条件下,有强氧化性,可以将SO2氧化成硫酸根,再与氯化钡产生硫酸钡白色沉淀,故C正确;
D.硫化钠溶液与SO2反应产生硫单质,有淡黄色沉淀,故D错误;
故选AC;
(3)x为SO32-,遇Cl2能被氧化成SO42-,SO42-遇盐酸酸化的氯化钡溶液,有白色沉淀产生,Cl2氧化SO32-的离子方程式为Cl2+SO32-+H2O=SO42-+2Cl-+2H+,故答案为:Cl2+SO32-+H2O=SO42-+2Cl-+2H+;
(4)SO2来制备硫酸,SO2被氧化,作还原剂,所以SO2在负极反应,其电极反应式为SO2-2e-+2H2O=SO42-+4H+;SO2制备硫酸,O2作氧化剂,电池的总反应式为2SO2+O2+2H2O=2H2SO4,故答案为:负;SO2-2e-+2H2O=SO42-+4H+;2SO2+O2+2H2O=2H2SO4.
点评:本题主要考查了二氧化硫的性质,涉及氧化还原反应、电化学知识,有一定的综合性,中等难度,解题时注意基础知识的运用和化学用语的规范表达.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A、CO2的电子式 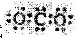 | ||
B、Cl-的结构示意图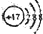 | ||
| C、H216O、D216O、H218O、D216O互为同素异形体 | ||
D、质量数为37的氯原子
|
在一种酸性溶液中可能存在Fe3+、NO
、Cl-、I-中的一种或几种离子,向该溶液中加入溴水,再加入淀粉,溶液变蓝.由此可推断溶液中( )
- 3 |
A、一定含有I-,一定没有NO
| ||
B、可能含有NO
| ||
C、可能含有NO
| ||
| D、一定含有Fe3+ |
 如图所示,50mL0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在装置中进行中和反应.通过测定反应过程中所放出的热量,可计算中和热,回答下列问题:
如图所示,50mL0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在装置中进行中和反应.通过测定反应过程中所放出的热量,可计算中和热,回答下列问题: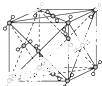 原子序数依次增大的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期.已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素中形成的单质中熔点最高;W原子核外的未成对电子数是前四周期元素中最多的.请回答下列问题:
原子序数依次增大的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期.已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素中形成的单质中熔点最高;W原子核外的未成对电子数是前四周期元素中最多的.请回答下列问题: