题目内容
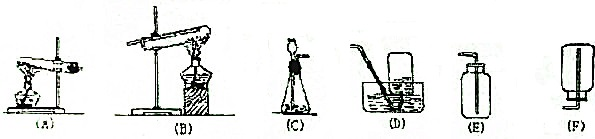
5.氮化硼(BN)是新型无机非金属材料,溶点3000℃,可以作润滑剂、高级耐火材料和超硬材料.某兴趣小组以下图装置用NH3与B2O3固体在高温下制备少量氮化硼.
(1)装置的连接顺序是Ⅰ-Ⅱ-Ⅲ-Ⅳ,则化合物X是氢氧化钙,装置Ⅱ中的药品和仪器是碱石灰 和干燥管.
(2)装置Ⅲ中发生反应的化学方程式是B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O.
(3)装置Ⅳ中广口瓶里盛装的是水,其作用是吸收未反应的氨气,进尾气的入口是b (填“a”或“b”)
(4)为防止装置内空气中的O2对制备反应的不利影响,则检验装置内空气被排尽的方法是先加入药品,连接装置Ⅰ、Ⅱ、Ⅲ,加热Ⅰ,用湿润的红色石蕊试纸在装置末导管口检验,若变蓝色,则说明空气已排尽.
(5)反应前瓷舟皿中盛有8.4g B2O3固体,反应结束后称得瓷舟皿中固体为6.4g,则氮化硼的产率为83.3%(保留百分号前一位小数).
(6)NH3与BCl3在高温下反应也能制备氮化硼,请从产物影响分析,工业上往往采用NH3与B2O3在高温下制备氮化硼的原因是用NH3与BCl3在高温下反应制备氮化硼的同时会产生氯化氢,氯化氢对设备腐蚀,导致成本升高.
分析 用NH3、B2O3为原料制备BN晶体,根据装置图可知,Ⅰ装置中用氯化铵与氢氧化钙产生氨气,经Ⅱ装置干燥后,氨气在管式电炉中与B2O3反应,生成BN,所以装置Ⅱ应为干燥管中加入碱石灰,反应中有氨气要用酸吸收,所以Ⅳ装置是吸收氨气尾气的装置,为防止倒吸,气体应从b导管进入,据此答题.
解答 解:用NH3、B2O3为原料制备BN晶体,根据装置图可知,Ⅰ装置中用氯化铵与氢氧化钙产生氨气,经Ⅱ装置干燥后,氨气在管式电炉中与B2O3反应,生成BN,所以装置Ⅱ应为干燥管中加入碱石灰,反应中有氨气要用酸吸收,所以Ⅳ装置是吸收氨气尾气的装置,为防止倒吸,气体应从b导管进入,
(1)根据上面的分析可知,化合物X是氢氧化钙,装置Ⅱ中的药品和仪器是 碱石灰 和干燥管,
故答案为:氢氧化钙;碱石灰;干燥管;
(2)装置Ⅲ中氨气与B2O3反应,生成BN,根据元素守恒可知,反应的化学方程式是B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O,
故答案为:B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O;
(3)氨气易溶于水,装置Ⅳ中广口瓶里盛装的是水,其作用是吸收未反应的氨气,为防止倒吸,气体应从b导管进入,
故答案为:吸收未反应的氨气;b;
(4)为防止装置内空气中的O2对制备反应的不利影响,可以用氨气排尽装置中的空气,则检验装置内空气被排尽的方法是先加入药品,连接装置Ⅰ、Ⅱ、Ⅲ,加热Ⅰ,用湿润的红色石蕊试纸在装置末导管口检验,若变蓝色,则说明空气已排尽,
故答案为:加热Ⅰ,用湿润的红色石蕊试纸在装置末导管口检验,若变蓝色,则说明空气已排尽;
(5)设实际产生BN的质量为xg,根据方程式B2O3+2NH3$\frac{\underline{\;高温\;}}{\;}$2BN+3H2O△m(固体),
50 20
x 8.4-6.4
则$\frac{50}{x}=\frac{20}{8.4-6.4}$,所以x=5,
根据元素守恒,8.4g B2O3固体理论上产生氮化硼的质量为$\frac{8.4}{70}×50$g=6g,所以氮化硼的产率为$\frac{5}{6}$×100%=83.3%,
故答案为:83.3%;
(6)用NH3与BCl3在高温下反应制备氮化硼的同时会产生氯化氢,氯化氢对设备腐蚀,导致成本升高,
故答案为:用NH3与BCl3在高温下反应制备氮化硼的同时会产生氯化氢,氯化氢对设备腐蚀,导致成本升高.
点评 本题主要考查物质的制备、分离提纯,难度中等,注意元素守恒思想的应用和实验基本操作的应用,可以培养学生综合分析问题和解决问题的能力.

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案| A. | 红色石蕊试纸 | B. | 碘化钾淀粉试纸 | C. | pH试纸 | D. | 蓝色石蕊试纸 |

| A. | N2(g)与O2(g)反应生成NO(g)是放热反应 | |
| B. | 2 mol O原子结合生成O2(g)时需要吸收498 kJ能量 | |
| C. | 1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量 | |
| D. | N2(g)+O2(g)=2NO(g)的反应热△H=+1444 kJ•molˉ1 |
| A. | 金属甲的阳离子比同价态的金属乙的阳离子氧化性强,则金属甲比金属乙活泼 | |
| B. | 原电池中电子从负极经过溶液流向正极 | |
| C. | 电解池中电解质溶液的阳离子向阴极迁移 | |
| D. | 在铁制品上镀银,铁做正极,银做负极 |
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD.
A.热裂解形成燃油
B.露天焚烧
C.作为有机复合建筑材料的原料
D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=64.39kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.84kJ•mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol•L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见表).
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率(10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+.
| A. | c(H+)=10-6 mol•L-1的溶液 | B. | pH<7的溶液 | ||
| C. | c(H+)>c(OH-)的溶液 | D. | 滴加酚酞显无色的溶液 |