题目内容
用铝箔包装0.1mol金属钠,用针扎若干小孔,放入水中,完全反应后,用排水取气法收集到气体(标准状况下)为
A.H2、O2混合气体 B.1.12L H2
C.>1.12L H2 D.<1.12L H2
C
【解析】
试题分析:发生的化学反应为2Na+2H2O = 2NaOH + H2↑ 2Al+2NaOH+2H2O=2NaAlO2 +3H2↑,
2 2 1 2 3
0.1mol 0.1mol 0.05mol 0.1mol 0.15mol
氢气的体积为 0.05mol×22.4L/mol=1.12L,所以最终收集到的气体为(标准状况)大于1.12L,选C。
考点:考查钠与铝的化学性质。

练习册系列答案
相关题目
(10分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |

(1)已知升高温度,NO2的浓度减小,则该反应是 热反应。
(2)下图中表示NO2的变化的曲线是 用O2表示从0~2 s内该反应的平均速率v =
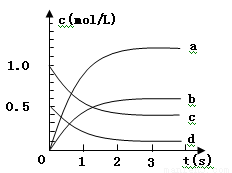
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
 B.
B.