题目内容
(10分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |

(1)已知升高温度,NO2的浓度减小,则该反应是 热反应。
(2)下图中表示NO2的变化的曲线是 用O2表示从0~2 s内该反应的平均速率v =
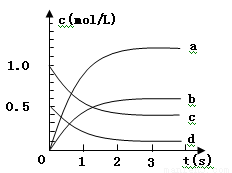
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(1)放 (2)b 0.15mol/(L·s) (3) c
【解析】
试题分析:(1)升高温度,NO2的浓度减小,说明平衡逆向移动,则该反应正反应是放热反应;
(2)根据表中数据可知,平衡是消耗NO是2mol-0.7mol=1.3mol,根据方程式可知,生成NO2 是1.3mol,浓度是0.65mol/L,则NO2的变化的曲线是b,用O2表示从0~2 s内该反应的平均速率v =(1.2÷2)mol/(2L×2s)= 0.15mol/(L·s)
(3)a及时分离出NO2气体,反应速率降低,错误;b.适当升高温度,反应速率加快,但平衡向逆反应方向移动,错误;c.增大O2的浓度,反应速率加快,平衡向正反应方向移动,正确;d.催化剂不能改变平衡状态,错误;选c。
考点:考查化学反应热量变化的判断,化学反应速率的计算,影响化学反应速率的因素等知识。

现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度 | 溶解性 |
乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水和酒精以任意比互溶 |
A.萃取法 B.结晶法 C.分液法 D.蒸馏法
 2C(g),若经 2 s(秒)后测得C的浓度为0.6 mol·L-1 ,现有下列几种说法,其中正确的是
2C(g),若经 2 s(秒)后测得C的浓度为0.6 mol·L-1 ,现有下列几种说法,其中正确的是