题目内容
下列是元素周期表的前三周期中的部分元素:
(1)这些元素中,最活泼的非金属元素是 ,最不活泼的元素是 ;(写元素名称)
(2)原子结构示意图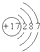 所表示的原子是 .(写元素符号)
所表示的原子是 .(写元素符号)
(3)⑧和⑨两种元素的最高价氧化物对应的水化物都是碱,分别写出这两种碱的化学式: 和 ;这两种碱的碱性强弱为:前者 后者 (填“大于”或“小于”);
(4)请写出由上表第三周期元素形成的一种离子化合物的化学式 .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | ② | ||||||
| 二 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 三 | ⑧ | ⑨ | ⑩ | (11) | ||||
(2)原子结构示意图
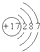 所表示的原子是
所表示的原子是(3)⑧和⑨两种元素的最高价氧化物对应的水化物都是碱,分别写出这两种碱的化学式:
(4)请写出由上表第三周期元素形成的一种离子化合物的化学式
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知,①为H、②为He、③为Li、④为C、⑤为N、⑥为O、⑦为F、⑧为Na、⑨为Mg、⑩为S、⑾为Cl,
(1)同周期自左而右非金属性最强、同主族自上而下非金属性减弱;稀有气体最不活泼;
(2)由原子结构示意图可知,该原子质子数为17,表示氯原子;
(3)⑧和⑨两种元素的最高价氧化物对应的水化物分别为NaOH、Mg(OH)2,同周期自左而右金属性减弱,金属性越强,最高价氧化物对应的水化物的碱性越强;
(4)上述第三周期元素中形成的离子化合物有NaCl等.
(1)同周期自左而右非金属性最强、同主族自上而下非金属性减弱;稀有气体最不活泼;
(2)由原子结构示意图可知,该原子质子数为17,表示氯原子;
(3)⑧和⑨两种元素的最高价氧化物对应的水化物分别为NaOH、Mg(OH)2,同周期自左而右金属性减弱,金属性越强,最高价氧化物对应的水化物的碱性越强;
(4)上述第三周期元素中形成的离子化合物有NaCl等.
解答:
解:由元素在周期表中的位置可知,①为H、②为He、③为Li、④为C、⑤为N、⑥为O、⑦为F、⑧为Na、⑨为Mg、⑩为S、⑾为Cl,
(1)同周期自左而右非金属性最强、同主族自上而下非金属性减弱,故F元素最活泼;稀有气体He,最不活泼,故答案为:氟;氦;
(2)由原子结构示意图可知,该原子质子数为17,表示氯原子,故答案为:Cl;
(3)⑧和⑨两种元素的最高价氧化物对应的水化物分别为NaOH、Mg(OH)2,同周期自左而右金属性减弱,金属性Na>Mg,金属性越强,最高价氧化物对应的水化物的碱性越强,故碱性:NaOH>Mg(OH)2,故答案为:NaOH;Mg(OH)2;大于;
(4)上述第三周期元素中形成的离子化合物有NaCl等,故答案为:NaCl等.
(1)同周期自左而右非金属性最强、同主族自上而下非金属性减弱,故F元素最活泼;稀有气体He,最不活泼,故答案为:氟;氦;
(2)由原子结构示意图可知,该原子质子数为17,表示氯原子,故答案为:Cl;
(3)⑧和⑨两种元素的最高价氧化物对应的水化物分别为NaOH、Mg(OH)2,同周期自左而右金属性减弱,金属性Na>Mg,金属性越强,最高价氧化物对应的水化物的碱性越强,故碱性:NaOH>Mg(OH)2,故答案为:NaOH;Mg(OH)2;大于;
(4)上述第三周期元素中形成的离子化合物有NaCl等,故答案为:NaCl等.
点评:本题考查元素周期表与元素周期律的综合应用,比较基础,侧重对基础知识的巩固,注意掌握把握元素周期表,注意对基础知识的全面掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质中属于电解质的是( )
| A、二氧化碳 | B、银 |
| C、硫酸钡 | D、烧碱溶液 |
下列各组离子,在水溶液中能大量共存的是( )
| A、K+、H+、SO42-、OH- |
| B、Na+、H+、Cl-、CO32- |
| C、Na+、Ca2+、NO3-、CO32- |
| D、Na+、Cu2+、Cl-、SO42- |