题目内容
某化学学习小组设计如图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质.
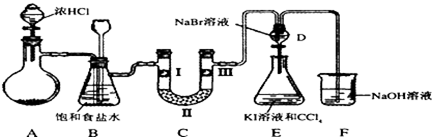
(1)若A装置中固体药品为MnO2,其化学方程式为
若A装置中固体药品为KClO3,则反应中每生成1molCl2时转移电子的物质的量为 mol.
(2)装置B的作用:
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是 .
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.但有同学认为该设计不够严密,他的理由可能 .
(5)请用化学方程式说明装置F的作用 .
(6)甲同学提出,装置F中改用过量的Na2SO3溶液,乙同学认认为此法不可行.请用离子方程式解释乙认为不可行的原因: .

(1)若A装置中固体药品为MnO2,其化学方程式为
若A装置中固体药品为KClO3,则反应中每生成1molCl2时转移电子的物质的量为
(2)装置B的作用:
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.但有同学认为该设计不够严密,他的理由可能
(5)请用化学方程式说明装置F的作用
(6)甲同学提出,装置F中改用过量的Na2SO3溶液,乙同学认认为此法不可行.请用离子方程式解释乙认为不可行的原因:
考点:氯气的实验室制法
专题:实验设计题
分析:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气;
依据氯酸钾中氯元素、氯化氢中氯元素化合价变化数目计算转移电子数;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,用饱和食盐水可以吸收氯化氢;B装置还能够检测实验过程中装置C是否发生堵塞;
(3)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(4)打开活塞,将装置D中少量溶液加入装置E中,生成的溴单质和碘化钾反应生成碘单质,当溴水浓度较小时,溶液颜色与氯水相似也呈黄色,由于过量的氯气也能够氧化碘离子,无法说明溴单质氧化性强于碘单质;
(5)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应,能够被氢氧化钠吸收;
(6)亚硫酸钠溶液中 通入氯气反应生成硫酸钠,同时生成的盐酸和亚硫酸钠反应会生成污染气体二氧化硫.
依据氯酸钾中氯元素、氯化氢中氯元素化合价变化数目计算转移电子数;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,用饱和食盐水可以吸收氯化氢;B装置还能够检测实验过程中装置C是否发生堵塞;
(3)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(4)打开活塞,将装置D中少量溶液加入装置E中,生成的溴单质和碘化钾反应生成碘单质,当溴水浓度较小时,溶液颜色与氯水相似也呈黄色,由于过量的氯气也能够氧化碘离子,无法说明溴单质氧化性强于碘单质;
(5)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应,能够被氢氧化钠吸收;
(6)亚硫酸钠溶液中 通入氯气反应生成硫酸钠,同时生成的盐酸和亚硫酸钠反应会生成污染气体二氧化硫.
解答:
解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气,化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
若A装置中固体药品为KClO3,和盐酸反应的化学方程式为:KClO3+6HCl=KCl+3Cl2↑+3H2O,反应生成3molCl2,转移电子5mol,则反应中每生成1mol Cl2时转移电子的物质的量为
,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,用饱和食盐水可以吸收氯化氢;
检测实验过程中装置C是否发生堵塞,若C中发生堵塞,会看的,B中长颈漏斗中液面上升,形成液柱;
故答案为:除去氯气中的氯化氢,检测实验过程中装置C是否发生堵塞;
3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,Ⅱ中应是干燥剂无水氯化钙,湿润的氯气通过干燥除去水分,通过Ⅲ处干燥的有色布条,布条不褪色;
故答案为:无水氯化钙,干燥的有色布条;
(4)打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,当溴水浓度较小时,溶液颜色与氯水相似也呈黄色,氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,所以该现象不能说明溴的非金属性强于碘;
故答案为:排除氯气对溴、碘的非金属性强弱实验的干扰;
(5)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(6)亚硫酸钠溶液中通入氯气反应生成硫酸钠,反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+,同时生成的盐酸和亚硫酸钠反应会生成污染气体二氧化硫,反应的离子方程式为SO32-+2H+=SO2↑+H2O,
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+,SO32-+2H+=SO2↑+H2O.
| ||
若A装置中固体药品为KClO3,和盐酸反应的化学方程式为:KClO3+6HCl=KCl+3Cl2↑+3H2O,反应生成3molCl2,转移电子5mol,则反应中每生成1mol Cl2时转移电子的物质的量为
| 5 |
| 3 |
故答案为:MnO2+4HCl(浓)
| ||
| 5 |
| 3 |
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,用饱和食盐水可以吸收氯化氢;
检测实验过程中装置C是否发生堵塞,若C中发生堵塞,会看的,B中长颈漏斗中液面上升,形成液柱;
故答案为:除去氯气中的氯化氢,检测实验过程中装置C是否发生堵塞;
3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,Ⅱ中应是干燥剂无水氯化钙,湿润的氯气通过干燥除去水分,通过Ⅲ处干燥的有色布条,布条不褪色;
故答案为:无水氯化钙,干燥的有色布条;
(4)打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,当溴水浓度较小时,溶液颜色与氯水相似也呈黄色,氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,所以该现象不能说明溴的非金属性强于碘;
故答案为:排除氯气对溴、碘的非金属性强弱实验的干扰;
(5)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(6)亚硫酸钠溶液中通入氯气反应生成硫酸钠,反应的离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+,同时生成的盐酸和亚硫酸钠反应会生成污染气体二氧化硫,反应的离子方程式为SO32-+2H+=SO2↑+H2O,
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+,SO32-+2H+=SO2↑+H2O.
点评:本题考查了氯气实验室制取、氯气性质的检验、实验设计、实验装置的理解评价、化学方程式、离子方程式的书写等,注意装置连接的操作和实验设计,掌握基础是关键,题目难度中等.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列实验过程中始终无明显现象的是( )
| A、二氧化碳通入硅酸钠溶液中 |
| B、二氧化碳通入氯化钙溶液中 |
| C、二氧化碳通入饱和的碳酸钠溶液中 |
| D、氨气通入氯化铝溶液中 |
设N为阿伏加德罗常数的数值,下列说法正确的是( )
| A、100mL lmol/LFeCl3溶液中含有Fe3+为0.1NA |
| B、80g CuO和Cu2S的混合物含有铜原子数一定为0.1NA |
| C、0.1mol冰醋酸和0.1mol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为0.1NA |
| D、2.24 L CH3CH3含有的分子数为0.1NA |
下列物质能与SiO2发生反应的是( )
①浓硫酸 ②H2O ③盐酸 ④HF ⑤KOH溶液 ⑥氧化钙.
①浓硫酸 ②H2O ③盐酸 ④HF ⑤KOH溶液 ⑥氧化钙.
| A、①②⑥ | B、②④ |
| C、④⑤⑥ | D、③④⑤⑥ |
同温同压下,等体积的两容器内分别充满14N16O和,13C16O气体,下列对两容器中气体判断正确的是( )
| A、质量相同 | B、分子数不同 |
| C、中子数相同 | D、质子数相同 |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、5.6gFe与足量氯气反应时失去的电子数为0.2NA | ||||
| B、常温常压下,4.8 g O2和O3的混合气体所含原子数为0.3NA | ||||
| C、0.3mol/LNa2SO4溶液中,所含Na+和SO42-总数为0.9NA | ||||
D、在反应2H2O2
|
 A、B、C、D均为中学化学常见的纯净物,A是单质,它们有如图反应关系.根据要求回答问题:
A、B、C、D均为中学化学常见的纯净物,A是单质,它们有如图反应关系.根据要求回答问题: