题目内容
用双线桥分析下列氧化还原反应化合价的变化,并填空.
(1)(双线桥)2KClO3
2KCl+3O2↑ 元素被氧化, 氧化产物.
(2)(单线桥)3Cl2+6NaOH
NaClO3+5NaCl+3H2O,Cl2是 剂, 还原产物.
(1)(双线桥)2KClO3
| ||
| △ |
(2)(单线桥)3Cl2+6NaOH
| ||
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)反应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价,转移电子数为12,据此分析;
(2)化合价降低元素所在的反应物是氧化剂生成还原产物,化合价升高元素所在的反应物是还原剂,反应中,化合价升高数目=化合价降低数目=转移电子数目.
(2)化合价降低元素所在的反应物是氧化剂生成还原产物,化合价升高元素所在的反应物是还原剂,反应中,化合价升高数目=化合价降低数目=转移电子数目.
解答:
解:(1)反应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价被氧化生成的氧气为氧化产物,转移电子数为12,用双线桥表示其电子转移情况为: ,
,
故答案为: ;O;O2.
;O;O2.
(2)反应3Cl2+6NaOH═5NaCl+NaClO3+H2O中,化合价升高的元素是Cl,失电子,所以Cl2是还原剂,化合价降低的元素也是氯元素,得到电子生成NaCl,所以Cl2也是氧化剂,NaCl为还原产物,化合价升高数目=化合价降低数目=转移电子数目=5,电子转移的方向和数目如下所示: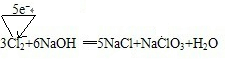 ,故答案为:
,故答案为: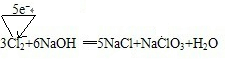 ,氧化剂和还原剂;NaCl.
,氧化剂和还原剂;NaCl.
 ,
,故答案为:
 ;O;O2.
;O;O2.(2)反应3Cl2+6NaOH═5NaCl+NaClO3+H2O中,化合价升高的元素是Cl,失电子,所以Cl2是还原剂,化合价降低的元素也是氯元素,得到电子生成NaCl,所以Cl2也是氧化剂,NaCl为还原产物,化合价升高数目=化合价降低数目=转移电子数目=5,电子转移的方向和数目如下所示:
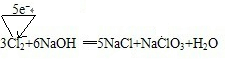 ,故答案为:
,故答案为: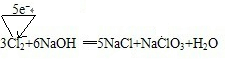 ,氧化剂和还原剂;NaCl.
,氧化剂和还原剂;NaCl.
点评:本题考查氧化还原反应,为高频考点,侧重于基本概念、电子转移表示方法的考查,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
下列除去杂质(括号内的物质为杂质)的方法中,错误的是( )
| A、FeCl3溶液(FeCl2):通入适量Cl2 |
| B、CO(CO2):通过NaOH溶液洗气后干燥 |
| C、SiO2(KCl):加水溶解后过滤、洗涤、干燥 |
| D、SO2(HCl):通过饱和Na2SO3溶液洗气后干燥 |
硅被誉为无机非金属材料的主角.据2001年12月的《参考消息》报道,有科学家提出硅是“21世纪的能源”“未来的石油”.下列有关说法正确的是( )
| A、硅的含量居第二位,在地球上有丰富的单质硅资源,如石英、水晶、玛瑙的主要成分都是单质硅 |
| B、硅相对于氢气便于运输、贮存,从安全角度考虑,硅是有开发价值的燃料 |
| C、存放NaOH溶液的试剂瓶应用细口玻璃瓶并配磨口玻璃塞 |
| D、硅是一种良好的半导体材料,所以是制造光导纤维的基本原料 |
反应2SO2+O2?2SO3经过一段时间后,SO3的浓度增加了0.4mol?L-1,在这段时间内用O2表示的反应速率为0.01mol?L-1?s-1,则这段时间为( )
| A、10 s |
| B、20 s |
| C、30 s |
| D、40 s |
下列说法不正确的是( )
| A、金属元素从化合态到游离态,该元素被还原 |
| B、非金属元素在化合物中可能呈现正价态 |
| C、金属阳离子被还原不一定得到金属单质 |
| D、金属单质在反应中只能作还原剂,非金属单质只能作氧化剂 |
下列过程中,没有发生化学变化的是( )
| A、溶洞中钟乳石的形成 |
| B、蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀 |
| C、干冰用于人工降雨 |
| D、豆科作物的根瘤菌对空气中氮的固定 |
 几种含硅元素的物质之间的相互转化关系如图所示,B是一种装饰品的主要成分,(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)
几种含硅元素的物质之间的相互转化关系如图所示,B是一种装饰品的主要成分,(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)